
| A. | 强电解质的导电性一定比弱电解质的导电性强 | |
| B. | 溶解度小的物质的导电性一定比溶解度大的物质的导电性弱 | |
| C. | 金属元素从化合态变为游离态时,该元素一定被还原 | |
| D. | 金属阳离子得电子多时氧化性强 |
分析 A、水溶液中导电能力与离子的浓度有关,浓度越大导电能力越强,浓度越小导电能力越弱;
B、溶液的导电能力取决于离子浓度的大小;
C、金属元素无负价;
D、氧化性的强弱取决于得电子的难易.
解答 解:A、溶液导电能力的强弱主要取决于溶液中的离子浓度与每个离子所带的电量.只有当两者乘积最大时,溶液导电能力越强.
水溶液中导电能力差的电解质不一定为弱电解质,如硫酸钡是强电解质,难溶于水,离子浓度小,导电能力弱,故A错误;
B、溶液的导电能力取决于离子浓度的大小,与物质的溶解度无关,故B错误;
C、金属元素无负价,故金属元素在化合态时一定为正价,则变为游离态时一定被还原,故C正确;
D、氧化性的强弱取决于得电子的难易,而非得电子的多少,故D错误.
故选C.
点评 本题考查了影响溶液的导电性因素和影响氧化性的因素,根据元素化合价变化来分析解答即可,难度不大,应注意的是溶液的导电能力取决于离子浓度的大小,与物质的溶解度和电解质的强弱无关.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:多选题
 如图是甲醇燃料电池的结构示意图.甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH30H+302→2C02+4H20.下列说法正确的是( )
如图是甲醇燃料电池的结构示意图.甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH30H+302→2C02+4H20.下列说法正确的是( )| A. | 左电极为电池的负极,a处通入的物质是甲醇 | |
| B. | 右电极为电池的负极,b处通入的物质是空气 | |
| C. | 负极反应式为:CH30H+H20-6e-→CO2+6H+ | |
| D. | 正极反应式为:02+2H20+4e-→40H- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
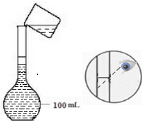
| 实验序号 | 5% H2O2溶液的体积(mL) | 选用试剂 | 选用试剂体积(mL) | 收集V mL O2所需时间(min) |
| ① | 10 | 蒸馏水 | 5 | m |
| ② | 10 | 0.1mol/L CuSO4 | v1 | n |
| ③ | 10 | 试剂M | 5 | p |
| ④ | 10 | 0.1mol/L Na2SO4 | 5 | m |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | C-O | C=O | H-O | C-H |
| E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
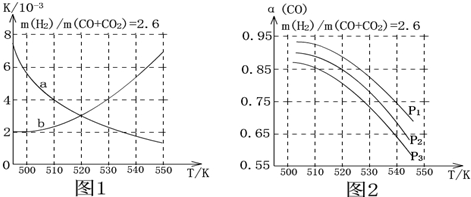
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该反应的化学方程式为:X+Y?2Z | |
| B. | 当反应速率大小关系为:v(X)=v(Y)=2v(Z)时,该反应达到平衡状态 | |
| C. | 图a中反应达到平衡时,Y的转化率为37.5% | |
| D. | 该反应的正反应是放热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com