
【题目】工业上常用水蒸气蒸馏的方法![]() 蒸馏装置如图
蒸馏装置如图![]() 从植物组织中获取挥发性成分。这些挥发性成分的混合物统称精油,大都具有令人愉快的香味。从柠檬、橙子和柚子等水果的果皮中提取的精油90%以上是柠檬烯
从植物组织中获取挥发性成分。这些挥发性成分的混合物统称精油,大都具有令人愉快的香味。从柠檬、橙子和柚子等水果的果皮中提取的精油90%以上是柠檬烯![]() 柠檬烯
柠檬烯![]()
![]() 。提取柠檬烯的实验操作步骤如下:
。提取柠檬烯的实验操作步骤如下:

①将1~2个橙子皮剪成细碎的碎片,投入乙装置中,加入约30mL水;
②松开活塞K。加热水蒸气发生器至水沸腾,活塞K的支管口有大量水蒸气冒出时旋紧,打开冷凝水,水蒸气蒸馏即开始进行,可观察到在馏出液的水面上有一层油层。
下列说法不正确的是( )
A.当馏出液油层无明显变化时,说明蒸馏完成
B.蒸馏结束后,先把乙中的导气管从溶液中移出,再停止加热
C.为完成实验目的,应将甲中的长导管换成温度计
D.要想从精油中得到柠檬烯,还要进行萃取、分液、蒸馏操作才能实现目的
科目:高中化学 来源: 题型:
【题目】下列实验方案中不能达到相应实验目的的是:
A | B | C | D | |
方案 |
| 在2mL1mol/LNaOH溶液中,加入5滴1mol/L氯化镁溶液,有白色沉淀,再加入5滴氯化铁溶液,观察沉淀颜色 | 实验室制备氢气,用粗锌代替纯锌与稀硫酸反应,反应速率加快 |
|
目的 | 探究浓度对化学反应速率的影响 | 探究沉淀溶解平衡的移动 | 探究形成原电池对反应速率的影响 | 探究温度对化学平衡的影响 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
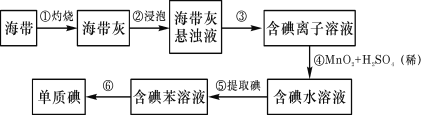
请填写下列空白:
(1)从海带中提取碘元素的步骤中,选用的实验仪器不能都用到的是____
①![]() ②
②![]() ③
③![]() ④
④![]() ⑤
⑤![]() ⑥
⑥![]() ⑦
⑦![]() ⑧
⑧
A.海带灼烧灰化,选用①②⑧ B.加水浸泡加热,选用②④⑦
C.过滤得到滤液,选用④⑤⑦ D.萃取和分液,选用③④⑥
(2)步骤⑤中,某学生选择用苯来提取碘水中的单质碘的理由是_____。(选填序号)
a.单质碘与苯不发生化学反应 b.碘在苯中溶解度小于水
c.碘在苯中溶解度大于水 d.苯与水互不相溶
提取碘的过程中,不能使用的有机溶剂是__________。(选填序号)
a.酒精 b.汽油 c.四氯化碳
(3)步骤④中MnO2的作用是__________(选填:氧化剂、还原剂、催化剂)。
(4)单质碘有许多用途,其中之一是生产加碘食盐中的碘剂——碘酸钾(KIO3)。合格加碘食盐含碘量(以I计)为20-50mg/Kg,则每千克该加碘食盐中碘酸钾的最小质量为_____ mg。
(5)已知:2Fe3++2I-=2Fe2++I2 氯气既可以氧化Fe2+,也可以氧化I-。往200mLFeI2溶液中通入8.96L(标准状况)Cl2,反应完成后,溶液中有![]() Fe2+被氧化,则原FeI2溶液的物质的量浓度_______。
Fe2+被氧化,则原FeI2溶液的物质的量浓度_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答问题:
Ⅰ.常温下,CaS的Ksp=10-8,饱和溶液中存在平衡: CaS(s)![]() Ca2+(aq)+S2-(aq)
Ca2+(aq)+S2-(aq)
(1)①该温度下,将10-4mol/L氯化钙溶液与2×10-4mol/L硫化钠溶液等体积混合,能否产生沉淀?答___;温度升高时,Ksp__(填“增大”、“减小”或“不变”下同)。
②滴加少量浓盐酸,c(Ca2+)___,原因是___(用文字和离子方程式说明)。
(2)若向CaS悬浊液中加入CuSO4溶液,生成一种黑色固体物质,写出该过程中反应的离子方程式___。
Ⅱ.(已知Ksp[Fe(OH)3]=10-38)若0.01mol/L FeCl3溶液中,如果要生成Fe(OH)3沉淀,应调整溶液pH,使pH___,若要使其沉淀完全,pH应___。(提示:填数据时,要有>,<,=)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌铁氧化还原液流电池工作原理如图所示

下列说法正确的是( )
A.膜X、膜Y分别是阴离子、阳离子交换膜
B.放电时,M极上的电势比N极上的高
C.放电时,负极电极反应式为:Zn+4OH--2e=Zn(OH)42-
D.充电时,阳极电极反应式为:Fe3++e-=Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图的各方框表示有关的一种反应物或生成物(某些物质已经略去),常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变蓝。

(1)写出下列各物质的化学式:X:______A:______C:______F:______。
(2)写出下列变化的化学方程式:
X![]() :______;
:______;
C→E:______;
F→G:______;
(3)检验X中阳离子的方法:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用乙醇制备溴乙烷:CH3CH2OH+HBr![]() CH3CH2Br+H2O,但通常采用溴化钠和浓硫酸与乙醇共热的方法。下面是某同学对该实验的猜想,你认为可能错误的是( )
CH3CH2Br+H2O,但通常采用溴化钠和浓硫酸与乙醇共热的方法。下面是某同学对该实验的猜想,你认为可能错误的是( )
A.制备过程中可能看到有气泡产生
B.可以将适量的NaBr、H2SO4(浓![]() 、CH3CH2OH三种药品置入一种容器中加热制备CH3CH2Br
、CH3CH2OH三种药品置入一种容器中加热制备CH3CH2Br
C.如在夏天做制备CH3CH2Br的实验,实际收集到的产物可能较少
D.为了除去CH3CH2Br中混有的HBr,可用热的NaOH溶液洗涤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NH3气体34 g,求:(注意书写单位)
(1)NH3的物质的量为__________________。
(2)NH3所含原子总数为__________________。
(3)这些NH3溶于150 mL水后形成溶液,密度为0.9281g/cm3,则其溶液的物质的量浓度为_______________。
(4)与___________gOH-有相同的电子数。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,一密闭容器中有如下反应:4CO(g)+2NO2(g) ![]() N2(g)+4CO2(g),下列叙述中不能说明该反应一定达到了平衡状态的是
N2(g)+4CO2(g),下列叙述中不能说明该反应一定达到了平衡状态的是
A.单位时间内有amolCO参加反应,同时也有amolCO2参加反应
B.NO2的生成速率:N2的消耗速率=2:1
C.CO的消耗速率:NO2的生成速率=2:1
D.NO2的消耗速率:CO2的消耗速率=1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com