
| A. | 2Al2O3(熔融)$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑ | B. | Fe2O3+2Al $\frac{\underline{\;高温\;}}{\;}$ 2Fe+Al2O3 | ||
| C. | Fe+CuSO4═FeSO4+Cu | D. | MgCl2(水溶液)$\frac{\underline{\;电解\;}}{\;}$ Mg+Cl2↑ |
分析 金属冶炼是工业上将金属从含有金属元素的矿石中还原出来的生产过程.金属的活动性不同,可以采用不同的冶炼方法,金属冶炼的方法主要有:
热分解法:对于不活泼金属,可以直接用加热分解的方法将金属从其化合物中还原出来(Hg及后边金属);
热还原法:在金属活动性顺序表中处于中间位置的金属,通常是用还原剂(C、CO、H2、活泼金属等)将金属从其化合物中还原出来(Zn~Cu);
电解法:活泼金属较难用还原剂还原,通常采用电解熔融的金属化合物的方法冶炼活泼金属(K~Al).
解答 解:A.Al是较活泼金属,工业上采用电解熔融氧化铝的方法冶炼,故A不选;
B.Fe的金属活动性处于中间位置,可以采用热还原法冶炼,可以采用铝热反应方法冶炼,故B不选;
C.Cu的金属活动性处于中间位置,可以采用热还原法冶炼,还可以采用湿法冶炼,用较活泼金属从铜盐溶液中置换出Cu,故C不选;
D.Mg是较活泼金属,应该采用电解熔融氯化镁的方法冶炼,如果电解氯化镁溶液,阳极上氯离子放电生成氯气、阴极上氢离子放电生成氢气,同时阴极附近生成氢氧根离子,镁离子和氢氧根离子反应生成氢氧化镁沉淀而得不到Mg,故D选;
故选D.
点评 本题考查金属的冶炼,明确金属活泼性强弱与冶炼方法的关系是解本题关键,根据金属的活泼性确定冶炼方法,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 装置 | 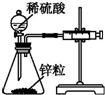 | 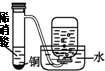 | 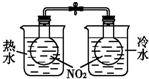 | 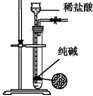 |
| 实验 | 结合秒表粗略测量锌与硫酸的反应速率 | 制备并收集少量NO气体 | 验证温度对化学平衡的影响 | 实验室随时制取少量CO2气体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纤维素和淀粉互为同分异构体 | |
| B. | 油脂发生皂化反应可生成脂肪酸和丙醇 | |
| C. | 酯类物质是产生水果香味的主要成分 | |
| D. | 糖类、蛋白质都属于天然高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | vA=0.5 mol•L-1•s-1 | B. | v B=0.5 mol•L-1•s-1 | ||
| C. | vC=0.4 mol•L-1•s-1 | D. | vD=1.2 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 部分卤代烃可用作灭火剂 | |
| B. | 福尔马林(甲醛溶液)可用于浸泡生肉及海产品以防腐保鲜 | |
| C. | 提倡人们购物时不用塑料袋,是为了防止白色污染 | |
| D. | 石油分馏是物理变化,可得到汽油、煤油和柴油等产品 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
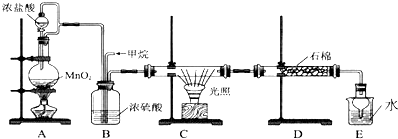
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式可表示为CH2CH2 | |
| B. | 苯、乙醇、乙酸都能发生取代反应 | |
| C. | 甲烷可以与氯气反应,而乙烯不能与氯气反应 | |
| D. | 液化石油气和天然气的主要成分都是甲烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
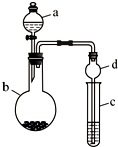 某课外小组同学设计了如图所示装置(夹持、加热仪器省略)进行系列实验.请根据下列实验回答问题:
某课外小组同学设计了如图所示装置(夹持、加热仪器省略)进行系列实验.请根据下列实验回答问题: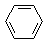 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$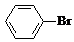 +HBr.向c中滴加AgNO3溶液,可观察到的现象是产生浅黄色沉淀.
+HBr.向c中滴加AgNO3溶液,可观察到的现象是产生浅黄色沉淀.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
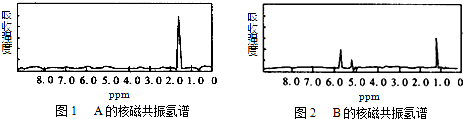
| A. | A是C3H6、B是C2H6 | B. | A是C6H6、B是C4H6 | C. | A是C6H6、B是C2H6 | D. | A是C3H8、B是C6H6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com