
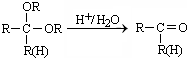
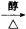 CH2=CHCHO+NaBr+H2O.
CH2=CHCHO+NaBr+H2O.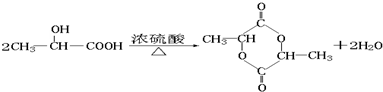 .
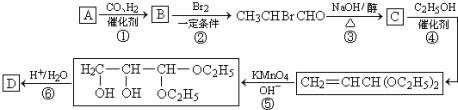
. 分析 由反应②B+Br2→CH3CHBrCHO可知,该反应为取代反应,故B为CH3CH2CHO,由反应①可知,A为CH2=CH2,由反应③CH3CHBrCHO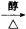 C,该反应为类似卤代烃的消去反应,故C为CH2=CHCHO,反应⑤在高锰酸钾碱性溶液氧化C=C双键,引入2个-OH,反应④的作用是保护醛基,防止反应⑤时被高锰酸钾碱性溶液氧化,由信息可知,反应⑥为醚键发生水解反应,重新生成醛基-CHO,故D为CH2(OH)CH(OH)CHO,以此解答该题.
C,该反应为类似卤代烃的消去反应,故C为CH2=CHCHO,反应⑤在高锰酸钾碱性溶液氧化C=C双键,引入2个-OH,反应④的作用是保护醛基,防止反应⑤时被高锰酸钾碱性溶液氧化,由信息可知,反应⑥为醚键发生水解反应,重新生成醛基-CHO,故D为CH2(OH)CH(OH)CHO,以此解答该题.
解答 解:由反应②B+Br2→CH3CHBrCHO可知,该反应为取代反应,故B为CH3CH2CHO,由反应①可知,A为CH2=CH2,由反应③CH3CHBrCHO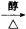 C,该反应为类似卤代烃的消去反应,故C为CH2=CHCHO,反应⑤在高锰酸钾碱性溶液氧化C=C双键,引入2个-OH,反应④的作用是保护醛基,防止反应⑤时被高锰酸钾碱性溶液氧化,由信息可知,反应⑥为醚键发生水解反应,重新生成醛基-CHO,故D为CH2(OH)CH(OH)CHO,
C,该反应为类似卤代烃的消去反应,故C为CH2=CHCHO,反应⑤在高锰酸钾碱性溶液氧化C=C双键,引入2个-OH,反应④的作用是保护醛基,防止反应⑤时被高锰酸钾碱性溶液氧化,由信息可知,反应⑥为醚键发生水解反应,重新生成醛基-CHO,故D为CH2(OH)CH(OH)CHO,
(1)由以上分析可知B为CH3CH2CHO,为丙醛,D为CH2(OH)CH(OH)CHO,故答案为:丙醛;CH2(OH)CH(OH)CHO;
(2)反应②是CH3CHBrCHO一定条件下与溴发生取代反应,反应⑤在高锰酸钾碱性溶液氧化C=C双键,引入2个-OH,故答案为:取代反应;氧化反应;
(3)反应③是CH3CHBrCHO在氢氧化钠醇溶液、加热条件下发生消去反应生成CH2=CHCHO,反应方程式为:CH3CHBrCHO+NaOH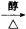 CH2=CHCHO+NaBr+H2O;
CH2=CHCHO+NaBr+H2O;
故答案为:CH3CHBrCHO+NaOH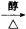 CH2=CHCHO+NaBr+H2O;
CH2=CHCHO+NaBr+H2O;
(4)反应⑤在高锰酸钾碱性溶液氧化C=C双键,引入2个-OH,反应④的作用是保护醛基,防止反应⑤时被高锰酸钾碱性溶液氧化;
故答案为:保护醛基,防止反应⑤时被高锰酸钾碱性溶液氧化;
(5)化合物M是CH2(OH)CH(OH)CHO的一种同分异构体,M在浓硫酸存在的条件下加热,既可以生成能使溴水褪色的化合物E(C3H4O2),又可以生成六原子环状化合物F(C6H8O4),故M中含有羟基-OH,羧基-COOH,它最早发现于酸牛奶中,是人体内糖类代谢的中间产物,故M为CH3CH(OH)COOH,E为CH2═CHCOOH,F为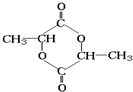 ,M→E的反应方程式为:CH3CH(OH)COOH$→_{△}^{浓硫酸}$CH2=CHCOOH+H2O,为消去反应,
,M→E的反应方程式为:CH3CH(OH)COOH$→_{△}^{浓硫酸}$CH2=CHCOOH+H2O,为消去反应,
故答案为:CH2═CHCOOH;消去反应;
(6)M→F的反应方程式为: ,
,
故答案为: .
.
点评 本题考查有机推断与合成,是对有机化合物知识的综合考查,有机推断几乎是高考不变的一个题型,每年高考中必考,根据转化关系推断B的结构是解题的关键,能较好的考查考生的阅读、自学能力和思维能力,难度中等.


科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质硅常用作半导体材料 | |
| B. | 硅酸钠是制备木材防火剂的原料 | |
| C. | 二氧化硅是制备光导纤维的基本原料 | |
| D. | 硅酸可由二氧化硅与水直接反应制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

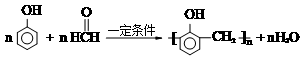 ,福尔马林是甲醛含量37%的水溶液,它的一个用途是浸制生物标本.
,福尔马林是甲醛含量37%的水溶液,它的一个用途是浸制生物标本.| 甲同学选择的试剂 | 乙同学认为不合理的理由 |
| 紫色石蕊试液 | |
| 新制氢氧化铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2 | B. | 2:5 | C. | 3:2 | D. | 4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol•L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
| c( S2O82-)/mol•L-1 | 0.040 | 0.040 | 0.080 | 0.080 | 0.040 |
| t/s | 88 | 44 | 22 | 11 | t1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com