
【题目】下列叙述错误的是( )
A.带相反电荷离子之间的相互作用称为离子键
B.金属元素与非金属元素化合时,不一定形成离子键
C.某元素的原子最外层只有一个电子,它跟卤素结合时所形成的化学键不一定是离子键
D.非金属元素原子间不可能形成离子键
科目:高中化学 来源: 题型:
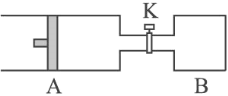
【题目】如图所示向A中充入1 mol X 、1 mol Y,向B中充入2 mol X、2 mol Y,起始时,
V(A) = V(B) = a L。在相同温度和有催化剂存在下,两容器中各自发生下述反应:X(g)+Y(g)![]() 2Z(g)+W(g) ΔH<0。达到平衡时,V(A) = 1.1a L。(连通管中气体体积不计)下列说法正确的是( )
2Z(g)+W(g) ΔH<0。达到平衡时,V(A) = 1.1a L。(连通管中气体体积不计)下列说法正确的是( )
A. n(Z)B = 2n(Z)A
B. A容器中X的转化率为20%
C. 若向A和B中均再加入1molX和1molY,X的体积分数均增大
D. 打开K保持温度不变,又达到平衡时,A的体积为3.3a L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,有关说法不正确的是( )

A. 元素b的单质不能与酸性氧化物发生化学反应
B. a、b、d、f四种元素的离子半径:f>d>a>b
C. 元素c的氧化物既能与酸反应又能与碱反应
D. a、c、e的最高价氧化物对应的水化物之间能够相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,pH = 2的CH3COOH和H2SO4溶液各1mL,分别加水稀释到1000 mL,其溶液的pH与溶液体积(V)的关系如图所示

(1)图中a点的值为_________________
(2)若对上述硫酸再稀释10000倍则溶液中n (H+) :n(SO42-)=_______
(3)在T℃时,醋酸的电离平衡常数K=1.0×10-5, Kw=1.0×10-13则下列反应CH3COO-+H2O![]() CH3COOH+OH- 的平衡常数K=_____________。
CH3COOH+OH- 的平衡常数K=_____________。
(4)在T℃时,取pH=2的硫酸溶液0.5VmL稀释到2VmL ,与0.1mol/L的NaOH溶液0.15VmL混合后稀释至10VmL,溶液的pH=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧乙酸(CH3COOOH)是无色透明液体,易溶于水、易挥发,见光易分解,具有强氧化性的高效消毒剂,使用过氧乙酸消毒剂时通常先用水稀释工业品过氧乙酸,然后用喷雾法对空气与地面进行消毒.
(1)配制220mL0.05mol/L的过氧乙酸溶液,需使用的仪器有:烧杯、量筒、玻璃棒及__________________、____________________;
(2)配制过程中,可能引起浓度偏高的操作有__________________
A.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
B.转移溶液时,不慎有少量溶液洒在容量瓶外
C.定容时,俯视容量瓶刻度线进行定容
D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,补充几滴水至刻度线
(3)过氧乙酸半小时内会完全分解成乙酸(CH3COOH)和一种常见的气体单质,检验该气体单质的实验方法是_____________________________.
(4)如果生产过氧乙酸的原料CH3COONa中混有了SO42﹣,要想除掉SO42﹣请选择下列试剂按照加入先后顺序填空__________________________________________(试剂不必选完,填序号即可)
①盐酸;②醋酸钡溶液;③氯化钡溶液;④醋酸;⑤碳酸钠溶液;⑥NaHCO3溶液.
(5)制取过氧乙酸反应原理为:H2O2+CH3COOH![]() CH3COOOH(过氧乙酸)+H2O,现称取5.0g用上述方法制取的过氧乙酸试样(液体),稀释至100mL备用.取上述稀释后过氧乙酸试样5.0mL,用0.01mol/L KMnO4溶液以除去其中的H2O2,随即加入10% KI溶液10 mL,摇匀(化学反应方程式为CH3COOOH+2KI=CH3COOK+I2+KOH)再将0.05mol/L Na2S2O3标准溶液加入到上述混合溶液中(化学反应方程式为:I2+2Na2S2O3=2NaI+Na2S4O6),消耗Na2S2O3标准溶液的总体积为20mL.通过计算确定原试样中过氧乙酸的质量分数为____________________.
CH3COOOH(过氧乙酸)+H2O,现称取5.0g用上述方法制取的过氧乙酸试样(液体),稀释至100mL备用.取上述稀释后过氧乙酸试样5.0mL,用0.01mol/L KMnO4溶液以除去其中的H2O2,随即加入10% KI溶液10 mL,摇匀(化学反应方程式为CH3COOOH+2KI=CH3COOK+I2+KOH)再将0.05mol/L Na2S2O3标准溶液加入到上述混合溶液中(化学反应方程式为:I2+2Na2S2O3=2NaI+Na2S4O6),消耗Na2S2O3标准溶液的总体积为20mL.通过计算确定原试样中过氧乙酸的质量分数为____________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镧系金属元素铈(Ce)常见有+3、+4两种价态,铈的合金耐高温,可以用来制造喷气推进器零件。请回答下列问题:
(1)雾霾中含有的污染物NO可以被含Ce4+的溶液吸收,生成NO2-、NO3- 物质的量之比为1:1,试写出该反应的离子方程式:______________________。
(2)用电解的方法可将上述吸收液中的NO2- 转化为稳定的无毒气体,同时生成Ce4+,其原理如下图所示。

①无毒气体从电解槽的_______(填字母代号)口逸出。
②每生成1mol无毒气体,同时可再生Ce4+ ______mol
(3)铈元素在自然界中主要以氟碳铈矿的形式存在,其主要化学成分为 CeFCO3。工业上利用氟碳铈矿提取CeCl3的一种工艺流程如下图所示
![]()

①焙烧过程中发生的主要反应的氧化剂和还原剂的物质的量之比为__________。
②向Ce(BF4)3中加入KCl溶液的目的是_________________________________。
③加热CeCl3·6H2O和NH4Cl的固体混合物可得固体无水CeCl3,其中NH4Cl的作用是_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度和压强相同时,在体积相同的两个密闭容器甲和乙,甲中充满O2气体,乙中充满O2和O3的混合气体,下列说法正确的是
A. 两容器中气体的质量相等 B. 两容器中气体的分子数目相等
C. 两容器中气体的氧原子数目相等 D. 两容器中气体的密度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度和有催化剂条件下,恒容密闭容器中发生反应N2+3H2 2NH3,下列说法正确的是( )
t/min | 0 | 5 | 10 | 15 | 20 |
c(NH3)/(mol·L-1) | 0 | 1.00 | 1.60 | 1.80 | 1.80 |
A. 0~10min内,v(NH3)=0.16mol·L-1·min-1 B. 0~10min内,v(N2)=0.18mol·L-1·min-1
C. 0~10min内,v(N2)=0.16mol·L-1·min-1 D. 15~20min内,反应v(N2)正= v(N2)逆=0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求写热化学方程式:
(1)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式__________。
(2)已知在25℃、101kPa下,1 g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出29.7 kJ的热量,试写出乙醇燃烧热的热化学方程式_______________。
(3)标准状况下,4.48L H2在足量O2中完全燃烧放出热量Q kJ,写出H2燃烧的热化学方程式_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com