

| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.7 | 9.6 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
| 温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
| Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
分析 β-锂辉矿(主要成分为LiAlSi2O6,还含有FeO、MgO、CaO等杂质)为原料来制取金属锂,加入过量浓硫酸溶解β-锂辉矿,加入碳酸钙除去过量的硫酸调节溶液PH=5,使铁离子和铝离子沉淀完全,加入水洗过滤洗去矿泥,然后加入氢氧化钙和碳酸钠沉淀镁离子和钙离子,过滤得到溶液中主要是锂离子的溶液,蒸发浓缩,加入碳酸钠沉淀锂离子生成碳酸锂,洗涤后加入盐酸溶解得到纯净的氯化锂溶液,加热蒸干得到氯化锂,电解熔融氯化锂得到金属锂,
(1)根据元素的化合价将Li、Al、Si写成氧化物形式,中间用•连接即可;
(2)根据工艺流程可知,加入碳酸钙目的是除去硫酸,调节溶液pH,除去铁离子、铝离子;
(3)反应Ⅲ要除去镁离子,加入过量氢氧化钙后生成氢氧化镁沉淀,然后用碳酸钠除去过量的钙离子杂质,所以沉淀为氢氧化镁、碳酸钙,据此写出反应的离子方程式;
(4)分离出不溶物方法为过滤;根据表中数据可知,Li2CO3在较高温度下溶解度小,用热水洗涤可减少Li2CO3的损耗;
(5)根据蒸干LiCl溶液时,LiCl有少量水解生成LiOH,氢氧化锂部分分解生成氧化锂,电解时会生成氢气.
解答 解:(1)将硅酸盐改为氧化物形式的方法为:依次将各元素写成氧化物形式,中间用“•”连接,同时要注意氧化物先后顺序,为Li2O•Al2O3•4SiO2,
故答案为:Li2O•Al2O3•4SiO2;
(2)由(1)改写可知,β-锂辉矿在加入过量浓硫酸后,只有SiO2不溶,同时Fe2+被氧化为Fe3+,并生成CaSO4沉淀,所以溶液中含有Fe3+、Al3+、Mg2+、Li+等离子,依据实验目的可知必须除去杂质离子,故在反应Ⅱ中加入碳酸钙的作用为:除去反应Ⅰ中过量的H2SO4;控制pH,使Fe3+、Al3+完全沉淀,
故答案为:除去反应Ⅰ中过量的H2SO4;控制pH,使Fe3+、Al3+完全沉淀;
(3)利用题干信息知反应Ⅲ要除去Mg2+,但在加入沉淀剂Ca(OH)2时会引入大量Ca2+,故还需加入Na2CO3除去Ca2+,即沉淀A为Mg(OH)2沉淀与CaCO3沉淀的混合物,反应的离子方程式为:Mg2++2OH-═Mg(OH)2↓、Ca2++CO32-═CaCO3↓,
故答案为:Mg2++2OH-═Mg(OH)2↓、Ca2++CO32-═CaCO3↓;
(4)实验室里分离固液混合物的操作是过滤,由题中给出Li2CO3的溶解度与温度的关系,可知洗涤Li2CO3沉淀要使用热水,
故答案为:过滤;热水;Li2CO3在较高温度下溶解度小,用热水洗涤可减少Li2CO3的损耗;
(5)由有氧气产生可逆推知可能的原因:加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解生成Li2O,电解时产生O2,
故答案为:加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解生成Li2O,电解时产生O2.
点评 本题考查了工业上以β-锂辉矿制取金属锂的方法,题目难度中等,试题涉及了化学式的书写、物质的分离与提纯、离子方程式的书写等知识,合理分析题中工艺流程是解题关键.


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:解答题

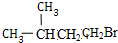 +NaOH$→_{△}^{乙醇}$
+NaOH$→_{△}^{乙醇}$ +NaBr+H2O;
+NaBr+H2O; +HBr$\stackrel{△}{→}$
+HBr$\stackrel{△}{→}$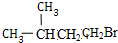 +H2O;
+H2O; ;
; 和
和 ;
;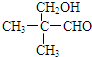 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阳光通过门缝有光亮通路 | |
| B. | 一支钢笔使两种不同牌号的墨水,容易出现堵塞 | |
| C. | 向氯化铁溶液中加 NaOH溶液,会出现红褐色沉淀 | |
| D. | 在河水与海水的交界处,易形成三角洲 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
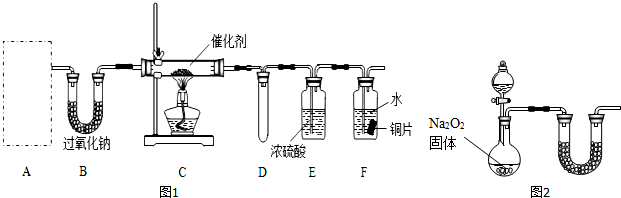
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
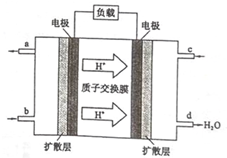 乙醇是一种常用的燃料,也可用于燃料电池.该燃料电池的工作原理如图所示.
乙醇是一种常用的燃料,也可用于燃料电池.该燃料电池的工作原理如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
.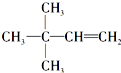 等.
等.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
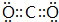 ;C 单质在高温下与B单质充分反应所得化合物的电子式为
;C 单质在高温下与B单质充分反应所得化合物的电子式为 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将过量NaOH溶液滴入Ca(HCO3)2溶液中:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 向硫酸铝铵[NH4Al(SO4)2]溶液中加入氢氧化钡溶液至SO42ˉ离子沉淀完全Al3++2SO42ˉ+2Ba2++4OHˉ═Al(OH)4ˉ+2BaSO4↓ | |
| D. | 向NH4HCO3溶液中加入过量的Ba(OH)2溶液并加热:Ba2++2OH-+NH4++HCO3-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+2H2O+BaCO3↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com