
| A、某微粒空间构型为三角锥形,则该微粒一定是极性分子 |
| B、某微粒空间构型为V形,则中心原子一定有孤电子对 |
| C、sp3杂化轨道是由同一个原子中能量相近的s轨道和p轨道混合起来形成的一组新轨道 |
| D、凡是中心原子采取sp3杂化轨道成键的分子其立体构型都是正四面体 |
| 1 |
| 2 |


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案科目:高中化学 来源: 题型:
| A、由于冰中的水分子间存在氢键,所以其密度大于液态水 |
| B、可以用氢键解释接近沸点的水蒸气的相对分子质量测定值比用化学式(H2O)计算出来的相对分子质量大 |
| C、分子间氢键和分子内氢键都会使熔沸点升高 |
| D、水加热到很高的温度都难以分解,这是由于氢键所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用锌粉代替锌粒 |
| B、改用3mol/L硫酸溶液 |
| C、改用热的2mol/L硫酸溶液 |
| D、向该硫酸溶液中加入等体积的水 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、S(s,单斜)=S(s,正交)△H=+0.33 kJ/mol |
| B、相同物质的量的正交硫比单斜硫所含有的能量高 |
| C、正交硫比单斜硫稳定 |
| D、①表示断裂1mol O2中的共价键所吸收的能量比形成lmolSO2中的共价键所放出的能量少297.16 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在pH等于2的醋酸溶液中加入少量0.01 mol?L-1的稀盐酸,溶液的pH会变小 | ||||
B、等物质的量浓度的碳酸钠溶液与碳酸氢钠溶液混合,混合溶液中c(CO
| ||||
| C、等浓度的CH3COOH和CH3COONa溶液按体积比2:1混合后的溶液中:2c(CH3COO-)+3c(OH-)=3c(H+)+c(CH3COOH) | ||||
| D、常温下,在50.00mLpH=b的NaOH溶液中滴入11.11mL pH=a的盐酸时,溶液pH变为2,则此NaOH溶液的pH为11(已知a+b=13,混合后溶液体积为61.11mL) |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在电解铝工业中添加冰晶石 |
| B、大力发展火电,缓解用电紧张 |
| C、开发太阳能、风能、氢能等清洁能源 |
| D、研制出性能优良的催化剂,降低反应所需温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 表示的粒子不会对水的电离平衡产生影响 表示的粒子不会对水的电离平衡产生影响 |
B、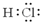 表示的物质加入水中,促进水的电离,c(H+)增大 表示的物质加入水中,促进水的电离,c(H+)增大 |
C、25℃时,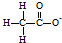 表示的微粒加入水中,促进水的电离,Kw不变 表示的微粒加入水中,促进水的电离,Kw不变 |
| D、水的电离程度只与温度有关,温度越高,电离程度越大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com