
| A、0 | B、1 | C、2 | D、3 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 实验步骤 | 解释或实验结论 |
| (1)测得A的蒸气密度是同状况下甲烷的4.375倍 | 试通过计算填空: (1)A的相对分子质量为 |
| (2)将此A 5.6g在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重7.2g和17.6g | (2)A的实验式是 (3)A的分子式为 |
| (3)将A通入溴水中,溴水褪色 | (4)说明A属于 |
(4)A的核磁共振氢谱如图: | (5)综上所述,A的结构简式为 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJ?mol-1 |
B、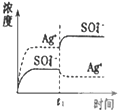 表示向Ag2SO4饱和溶液中加入等体积Na2SO4稀溶液,平衡会向左移动,Ksp减小 |
C、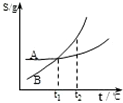 表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数B>A |
D、 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去乙烷中混有的乙烯的方法是通氢气在一定条件下反应,使乙烯转化为乙烷 |
| B、苯、溴苯在常温、常压下为无色且密度比水小的液体 |
| C、丙烯与2-丁烯都存在順反异构体 |
| D、苯不能与溴水发生加成反应,也不能被酸性KMnO4溶液氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等温浓度均为0.1mol?L-1的HA、HB溶液中,其溶液的pH大小为:pH(HA)>pH(HB) |
| B、在0.1mol?L-1的NaA溶液中各离子浓度关系为:c(Na+)>c(A-)>c(OH-)>c(H+) |
| C、等体积pH相同的HA、HB溶液,分别加入等浓度的NaOH溶液,恰好完全反应消耗的NaOH溶液体积HA比HB多 |
| D、等温浓度均为0.1mol?L-1的NaA、NaB溶液中,其溶液的pH大小为:pH(NaA)>pH(NaB) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在含Fe3+、Cu2+、H+的溶液中加入锌粉:Cu2+、Fe3+、H+ |
| B、在含I-、SO32-、Br-的溶液中不断通入氯气:I-、Br-、SO32- |
| C、在含AlO2-、SO32-、OH-的溶液中逐滴加入硫酸氢钠溶液:OH-、AlO2-、SO32- |
| D、在含Fe3+、H+、NH4+的溶液中逐渐加入烧碱溶液:H+、NH4+、Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯碱、烧碱都属于碱类 |
| B、冰和干冰既是纯净物又是化合物 |
| C、铅笔芯、铅球主要成分都是铅 |
| D、液氯和氯水是同一种物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、胶体能发生电泳现象是因为胶体带电 |
| B、生石灰与水混合的过程只发生物理变化 |
| C、O3是由3个氧原子构成的化合物 |
| D、CuSO4?5H2O是一种混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子的结构是由键角决定的 |
| B、共价键的键能越大,共价键越牢固 |
| C、CF4、CCl4、CBr4、CI4中C-X键的键长、键角均相等 |
| D、H2O分子中的两个O-H键的键角为180° |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com