
【题目】钠和铝均是重要的金属。
(1) 铝的原子结构示意图是___________________。
(2) 铝与NaOH溶液反应的离子方程式为______________________________;
(3)同温同压下,在体积和浓度均为100 mL 0.2 mol·L-1的盐酸及NaOH溶液中各加入等质量的Al, 产生气体的体积之比为5∶6,则所加Al的质量为______________。
(4) 过氧化钠可做呼吸面具的供氧剂,其中Na2O2与CO2反应的化学方程式为________________。
【答案】 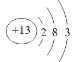 2Al + 2OH- + 2H2O ═ 2AlO2- + 3H2↑ 0.216 g 2Na2O2 + 2CO2 ═ 2Na2CO3 + O2
2Al + 2OH- + 2H2O ═ 2AlO2- + 3H2↑ 0.216 g 2Na2O2 + 2CO2 ═ 2Na2CO3 + O2
【解析】本题主要考查钠和铝的性质。
(1)铝的原子结构示意图是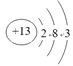 。
。
(2)铝与NaOH溶液反应的离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑;
(3)a.2Al+6HCl![]() 2AlCl3+3H2↑,b.2Al+2NaOH+2H2O
2AlCl3+3H2↑,b.2Al+2NaOH+2H2O![]() 2NaAlO2+3H2↑。HCl和NaOH的物质的量均为0.2mol。同温同压下氢气的物质的量之比等于体积之比为5∶6。若HCl和NaOH完全反应,则产生氢气的物质的量之比为1:3;若铝完全反应,则产生氢气的物质的量之比为1:1。实际产生氢气的物质的量之比为5:6,说明反应a剩余铝,HCl完全消耗,反应b剩余氢氧化钠,铝完全消耗。根据反应a和反应b产生氢气的物质的量之比为5:6,得到反应a中HCl与反应b中铝的关系为10HCl~4Al,因此,所加Al的物质的量为0.08mol,所加Al的质量为0.08mol×27g/mol=0.216g。
2NaAlO2+3H2↑。HCl和NaOH的物质的量均为0.2mol。同温同压下氢气的物质的量之比等于体积之比为5∶6。若HCl和NaOH完全反应,则产生氢气的物质的量之比为1:3;若铝完全反应,则产生氢气的物质的量之比为1:1。实际产生氢气的物质的量之比为5:6,说明反应a剩余铝,HCl完全消耗,反应b剩余氢氧化钠,铝完全消耗。根据反应a和反应b产生氢气的物质的量之比为5:6,得到反应a中HCl与反应b中铝的关系为10HCl~4Al,因此,所加Al的物质的量为0.08mol,所加Al的质量为0.08mol×27g/mol=0.216g。
(4)过氧化钠可做呼吸面具的供氧剂,其中Na2O2与CO2反应的化学方程式为2Na2O2+2CO2═2Na2CO3+O2。


科目:高中化学 来源: 题型:
【题目】随着环境问题的日益严重,垃圾的处理问题正日益被人们所重视.某垃圾处理厂对金属垃圾(主要成分是铁、铜、氧化铁、二氧化硅)处理及综合利用的部分工艺如图所示.请回答下列问题:
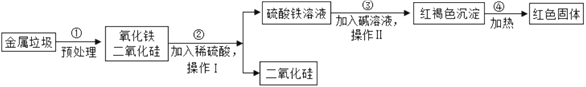
(1)I、II均含有_____操作,此操作中玻璃棒的作用是搅拌、____。操作II完成后红褐色沉淀洗涤的具体操作为_______。
(2)步骤③所发生的反应属于基本反应类型中的______。
(3)请写出步骤②、④所发生反应的化学方程式:
②_____________________________④ ____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下1molC3H8发生如下反应:①C3H8→C2H4+CH4②C3H8→C3H6+H2如果C3H8的转化率为80%,且混合气体中m(CH4)=m(H2),则下列说法正确的是( )
A. 反应后混合气体的平均相对分子质量为35.2
B. 两种烯烃物质的量之比,即n(C2H4)/n(C3H6)为1∶1
C. 将混合气体通入溴的四氯化碳溶液,溶液增重128g
D. 两种烯烃物质的量之和,即n(C2H4)+n(C3H6)为0.8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关NaHCO3和Na2CO3的下列叙述中错误的是( )
①等质量的NaHCO3和Na2CO3分别与足量盐酸反应,Na2CO3产生的CO2多
②84 g NaHCO3、106 g Na2CO3分别与足量的盐酸完全反应,Na2CO3消耗盐酸的物质的量是NaHCO3的两倍
③将澄清石灰水分别倒入两种盐溶液中,只有Na2CO3溶液中产生白色沉淀
④通常状况下,相同温度下,Na2CO3的溶解度大于NaHCO3
A. ①② B. ②③ C. ②④ D. ①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列三组物质中,均有一种物质的类别与其它三种不同
A.MgO、Na2O、CO2、CuO B.HCl、H2O、H2SO4、HNO3 C.NaOH、Na2CO3、KOH、Cu(OH)2
(1) 三种物质依次是(填化学式):A______________;B_______________;C________________。
(2) 这三种物质相互作用可生成一种新物质NaHCO3,该反应_______(“是”或“不是”)氧化还原反应。
(3) 写出物质C与足量稀硫酸反应的离子方程式:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,反应物的用量或浓度改变时,不会改变生成物的是
A. 铜与硝酸反应 B. 明矾溶液与烧碱溶液反应
C. 碳酸钠溶液和盐酸反应 D. 硫在氧气中燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.含有非极性键的分子一定是非极性分子B.非极性分子中一定含有非极性键
C.由极性键形成的双原子分子一定是极性分子D.键的极性决定了分子的极性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是教材中实验装置。

回答下列问题:
(1)甲仪器的名称是______,与同类仪器相比其优点是______、______。
(2)向乙通水,进水口是_______(填“a”或“b”),理由是_____________________。
(3)利用上述装置进行醇与酸的酯化反应。
①醇、酸、酯和水之间的沸点满足的条件是___________。
②如果外接一个装置可以满足蒸馏的条件,那么,此时醇、酸、酯和水之间的沸点满足的条件是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA 表示阿伏加德罗常数的值,下列说法正确的是
A. 44.8LH2完全燃烧消耗氧气分子数为NA
B. 28g乙烯(C2H4)和丙烯(C3H6)的混合物含碳原子数为2.5NA
C. 2mol·L-1NaOH溶液中的钠离子数为2NA
D. 1molD2O和H218O混合物中子数为10NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com