
J��M��R��T��ԭ��������������Ķ���������Ԫ�أ�J��R�����ڱ��е����λ�����±����� ֪JԪ��������ϼ۵ľ���ֵ����ԭ��������������ȣ�M�ǵؿ��к������Ľ���Ԫ�ء�����˵��������ǣ� ��
A��J������ɵ���̬�⻯������п���ֻ���м��Թ��ۼ�
B��M������������������Һ��Ӧ������һ�ֿ�ȼ������
C��R��T��Ԫ�ص���̬�⻯���У�R����̬�⻯����ȶ�
D��J��M��R��TԪ������������Ӧ��ˮ������������ǿ����HTO4

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NA��ʾ�����ӵ�����������˵����ȷ����
A����1 L 2 mol/L��FeCl3��Һ�Ƴɽ�������к�����������������Ϊ2NA
B��1 L 0.1 mol/L NaHSO4��Һ�к���0.1 NA��HSO4-
C�����³�ѹ�£�23 g NO2��N2O4�Ļ������һ������NA����ԭ��
D��1 mol��������ϡ���ᷴӦת�Ƶĵ�����ĿΪ3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ʵ��װ�úͷ���������Ӧʵ�飬�ܴﵽʵ��Ŀ�ĵ���
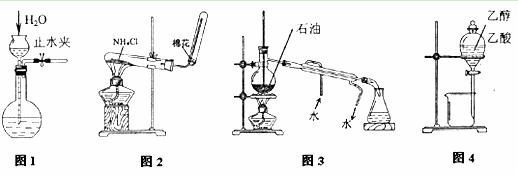
A����ͼ1��ʾ�������װ�õ������� B����ͼ2��ʾװ�úͷ�����ȡ����
C����ͼ3��ʾװ�úͷ�������ʯ�ͷ��� D����ͼ4װ�úͷ��������Ҵ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1����þ������Ԫ���е�һ������������ ����Ԫ�����ƣ���
��2��ij�����������Ӻ�������Ų�ʽΪ��Ar��3d54s0,�ý�����Ԫ�ط���Ϊ ��
��3��������ڷǼ��Լ�����λ������������»������� ��
A�� NH4Cl���� B�� Na3AlF6���� C�� Na2CO3•10H2O����
D�� CuSO4��Һ E�� CH3COOH��Һ
��4�����ֹ��ۼ������������±���
| �� | H-H | N-H | N-N | N=N | N��N |
| ����/kJ•mol-1 | 436 | 391 | 159 | 418 | 945 |
�����ϱ��������㲢д�������ֽ�Ϊ�������������Ȼ�ѧ����ʽ��
��
��5���Ҵ���������ͬ���칹�壬���������ʴ��ڲ��죺
| ����ʽ | �ṹ��ʽ | �۵� | �е� | ˮ���� | |
| �Ҵ� | C2H6O | C2H5OH | -114��3�� | 78��4 ��C | ���� |
| ������ | C2H6O | CH3OCH3 | -138��5�� | -24��9�� | �� |
�Ҵ��Ͷ����ѷе㼰ˮ���Բ������Ҫԭ���� ��
��6������ͭ������Ũ��ˮ��˫��ˮ�Ļ����Һ����������ɫ��Һ��������ɫ��Ũ��Һ�м����Ҵ��ɼ�������ɫ�����������뻭��������ɫ�����ӵĽṹ��ʽ ��
��7��ʯīϩ��Ӧ��Ϊ������ҵ�ķ�չ�������ش��ͻ�ƣ���ṹ���Կ����ǵ����ʯī������̼ԭ�ӵ��ӻ���ʽΪ ��C60�ľ���ṹ�����ڸɱ�����ÿ��C60����������Ϊ (�ú�NA��ʽ�ӱ�ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������Һ�У��ܴ���������������ǣ� ��
A.��ʹpH��ֽ����ɫ����Һ�У�K+��Ba2+��H+��Br-
B. ����Al�ܷų�H2����Һ�У�K+��Na+��NO3-��Cl-
C.���д���Fe3+����Һ�У�SCN-��I-��K+��Br-
D.��ʹʯ����Һ�Ժ�ɫ����Һ�У�K+��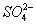 ��S2-��
��S2-��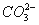
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ijһ���ӷ�Ӧ��ϵ�з�Ӧ��Ͳ��ﹲ�������֣�
MnO4-��H+��O2��H2O��H2O2��Mn2+��
��֪�÷�Ӧ�е�H2O2ֻ�������¹��̣�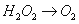
��1���÷�Ӧ�еĻ�ԭ���� ����ԭ������________��
��2��KMnO4��Һ�������Ե���ǿ�����Բ�����ǿ��Ӧѡ��_______��ѡ�ϡ���ᡱ��Ũ���ᡱ������KMnO4��Һ���ữ��
��3�����練Ӧת����0.3mol���ӣ�������������ڱ�״�������Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͬ�����������ͳ����У�����ԭ�Ӹ���ǰ������ߵĹ�ϵΪ������ ��
����A�����ڡ��� B��С�ڡ��� C�����ڡ� ��D������ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�Ȼ�þ��Һ���ܶ�Ϊ1.18 g��cm��3������þ���ӵ���������Ϊ5.1%,300 mL����Һ��Cl�������ʵ���Լ����(����)
A��0.37 mol B��0.63 mol
C��0.74 mol D��1.5 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
FeS��һ��Ũ�ȵ�HNO3��Ӧ������Fe(NO3)3��Fe2(SO4)3��NO2��N2O4��NO��H2O����NO2��N2O4��NO�����ʵ���֮��Ϊ1�U1�U1ʱ��ʵ�ʲμӷ�Ӧ��FeS��HNO3�����ʵ���֮��Ϊ�� ��
A��1��6 B��1��7 C��2��11 D��16��25
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com