
实验探究:探究碳、硅元素的非金属性的相对强弱
根据要求完成下列各小题
(1)实验装置:
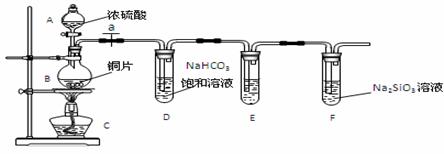
填写所示仪器名称A B
(2)实验步骤:
连接仪器、_____________、加药品后,打开a、然后滴入浓硫酸,加热
(3)问题探究:(已知酸性强弱:亚硫酸 >碳酸)
①铜与浓硫酸反应的化学方程式是 ;
装置E中足量酸性KMnO4溶液的作用是 ;
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是 ;
③依据试管D中的实验现象,能否证明硫元素的非金属性强于碳元素的非金属性___(填“能”或“否”),试管D中发生反应的离子方程式是
科目:高中化学 来源: 题型:
四种主族元素的离子aXm+、bYn+、cZn-和dRm-(a、b、c、d为元素的原子序数),它们具有相同的电子层结构,若m>n,则对下列叙述的判断正确的是
①a-b=m-n ②元素的原子序数a>b>c>d
③元素非金属性Z>R ④最高价氧化物对应水化物的碱性X>Y
A.②③ B.③
C.①②③④ D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
为说明氯比硫的非金属性强,下列事实可作依据的是( )
A.HCl的溶解性强于H2S B.氯的最高价为+7价
C.H2S中的S2-能被Cl2氧化 D.HClO的氧化性强于H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学用语使用正确的是( )
A. 硫原子的原子结构示意图:
B.NH4Cl的电子式: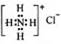
C.原子核内有10个中子的氧原子:
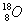
D.纯碱的化学式为NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.常温下醋酸分子不可能存在于pH>7的碱性溶液中
B.常温下向氯化铵溶液中加入少量氨水使溶液的pH=7,则混合溶液中c(Cl-)>c(NH4+)
C.0.1 mol·L-1的氯化铵溶液与0.05 mol·L-1的氢氧化钠溶液等体积混合,溶液中离子浓度c(Cl-)>c(NH4+)>c(Na+)>c(OH-)
D.0.1 mol·L-1硫化钠溶液中离子浓度关系c(OH-)=c(H+)+c(HS-)+c(H2S)
查看答案和解析>>
科目:高中化学 来源: 题型:
设阿伏加德罗常数为NA,下列说法正确的是
A.5.6g铁粉与足量Cl2反应,失去的电子数为0.2NA
B.1mol NH3含有的电子数10NA
C.常温常压下,22.4 L的氧气含氧原子数为2NA
D.常温下,1 L0.1mol·L-1AlCl3溶液中含Al3+数为0.1 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,U型管的左端被水和胶塞封闭有甲烷和氯气(体积比为1︰4)的混和气体,假定氯气在水中溶解度可以忽略。将该装置放置在
有光亮的地方,让混和气体缓慢地反应一段时间。
⑴ 假设甲烷与氯气充分反应,且只产生一种有机物,请写出化学方程式。 。
⑵ 经过几个小时的反应后,U型管右端的玻璃管中水柱变化是 。
A.升高 B.降低 C.不变 D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com