
| A. | 光导纤维、聚酯纤维、棉花都属于高分子化合物 | |
| B. | 在大米酿酒的过程中,淀粉最后变成了单糖 | |
| C. | 泡沫灭火器中用的是苏打和硫酸铝 | |
| D. | 海轮外壳上镶入锌块,可减缓船体的腐蚀 |
分析 A.高分子化合物,是指那些由众多原子或原子团主要以共价键结合而成的相对分子量在一万以上的化合物.按来源分类可把高分子分成天然高分子和合成高分子两大类;
B.淀粉水解生成葡萄糖,葡萄糖分解生成酒精;
C.泡沫灭火器的药品是碳酸氢钠和硫酸铝;
D.锌比铁活泼,可做原电池的负极.
解答 解:A.聚酯纤维是化学纤维的一种属于合成高分子,棉花属于天然高分子,两者都属于高分子化合物,光导纤维主要成分是二氧化硅,不是高分子化合物,故A错误;
B.淀粉水解生成葡萄糖,葡萄糖分解生成酒精,故B错误;
C.泡沫灭火器的药品是碳酸氢钠和硫酸铝,碳酸氢钠和硫酸铝反应生成大量的二氧化碳,其反应速率比碳酸钠和硫酸铝反应速率大,故C错误;
D.锌比铁活泼,可做原电池的负极,保护铁不被氧化,此为牺牲阴极的阳极保护法,故D正确;
故选D.
点评 本题考查较为综合,侧重于化学与生活、环境的考查,为高频考点和常见题型,有利于培养学生良好的科学素养,提高学习的积极性,题目难度不大,注意相关基础知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | 磁性氧化铁溶于稀硝酸:Fe3O4+8H+=Fe2++2Fe3++4H2O | |
| B. | Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++HCO3-+OH-=CaCO3↓+H2O | |
| C. | 用两根铜棒电解稀盐酸:2H++2Cl-$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑ | |
| D. | Na2S2O3溶液中加入稀硫酸:2S2O+4H+═SO42-+3S↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | A | B | C | D | E | F | G | H |
| 原子半径(nm) | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 | 0.152 | 0.037 | 0.099 |
| 主要化合价 | +2 | +3 | +2 | +6,-2 | -2 | +1 | +1,-1 | +7,-1 |
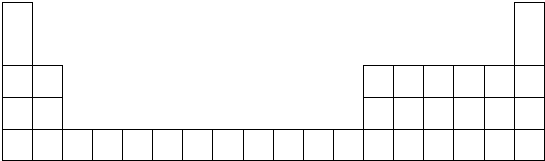
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢键不是化学键 | |
| B. | HF的稳定性很强,是因为其分子间能形成氢键 | |
| C. | 乙醇分子与水分子之间只存在范德华力 | |
| D. | 碘化氢的沸点比氯化氢的沸点高是由于碘化氢分子之间存在氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④⑤ | B. | ①②③④⑤ | C. | ②③④ | D. | ②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
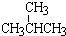 和
和 ; ⑧
; ⑧
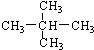 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 表示的分子式C6H14;名称是2-甲基戊烷.
表示的分子式C6H14;名称是2-甲基戊烷.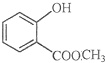 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大体系压强 | B. | 升温 | C. | 加入铁触媒 | D. | 减小NH3的浓度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com