
 草酸亚铁晶体(FeC2O4•2H2O)呈淡黄色.某课题组为探究草酸亚铁晶体的化学性质,进行了一系列实验探究.
草酸亚铁晶体(FeC2O4•2H2O)呈淡黄色.某课题组为探究草酸亚铁晶体的化学性质,进行了一系列实验探究.| 实验步骤(不要求写出具体操作过程) | 预期实验现象和结论 |
| 取少量黑色固体 |
分析 (1)向盛有草酸亚铁晶体的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现溶液颜色逐渐变为棕黄色,并检测到CO2生成.说明草酸亚铁被氧化为铁离子、二氧化碳气体,草酸亚铁具有还原性,依据电子守恒计算得到消耗的高锰酸钾物质的量;
(2)草酸亚铁晶体可完全分解,生成几种氧化物,残留物为黑色固体可能为氧化亚铁或四氧化三铁,分析判断;
(3)【定性研究】氧化亚铁溶解于盐酸生成氯化亚铁溶液,加入KSCN溶液,若溶液不变红证明假设一正确;
【定量研究】根据图中提供的信息,通过计算可以判断反应的化学方程式和物质的化学式.
解答 解:(1)高锰酸钾溶液的紫红色褪去,溶液变为棕黄色,很显然是FeC2O4被高锰酸钾氧化为Fe3+的结果,表明FeC2O4具有还原性.分析有关元素化合价的变化可知,反应过程中1 mol FeC2O4•2H2O可失去3 mol电子,而l mol KMnO4可得到5 mol电子,根据得失电子数相等的原则,反应中FeC2O4•2H2O与KMnO4的物质的量之比为5:3.因此,若反应中消耗1 mol FeC2O4•2H2O,则参加反应的KMnO4为0.6 mol,
故答案为:还原性;0.6;
(2)铁的氧化物中,呈黑色的有FeO和Fe3O4,假设二:全部是Fe3O4;假设三:是FeO和Fe3O4的混合物,
故答案为:全部是Fe3O4;是FeO和Fe3O4的混合物;
(3)【定性研究】FeO与盐酸或硫酸反应生成Fe2+,Fe2+与KSCN不反应.但Fe3O4或FeO和Fe3O4的混合物溶于稀盐酸或稀硫酸中生成Fe3+,遇KSCN变红色.据此即可设计方案进行验证,
故答案为:取少量黑色固体,加入适量稀盐酸(或稀硫酸)溶解,在溶液中加入KSCN溶液;
预期实验现象和结论:若溶液不变红色,则假设一成立;若溶液变红色,则假设一不成立;
【定量研究】草酸亚铁品体受热首先失去结品水,得到FeC2O4(即A点对应物质).400℃时固体质量减少,应该是FeC2O4发生分解,牛成铁的氧化物(即B点对应物质).根据图象可知1.0 g晶体分解生成的铁的氧化物的质量为0.4 g.设此铁的氧化物的化学式为FeaOb,
根据Fe守恒可知0.4 g此氧化物中铁元素的质量为1.0 g×$\frac{56}{180}$,
氧元素的质量为(0.4g-1.0 g×$\frac{56}{180}$)g,故a:b=(1.0g×$\frac{56}{180}$):(0.4g-1.0 g×$\frac{56}{180}$),
解得a:b=1:1,
即晶体分解所得铁的氧化物为FeO,
故答案为:FeO.
点评 本题考查了铁及其化合物性质的实验验证和实验分析判断,定量计算,图象分析是解题关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题

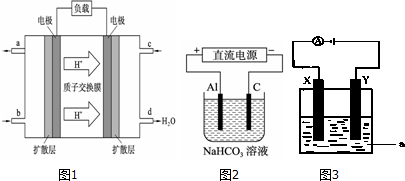
| A. | M是直流电的正极 | B. | 电子流向是N→b→a→M | ||
| C. | 电解过程中,水是氧化剂 | D. | b电极附近溶液的pH变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食盐加碘所添加的是碘酸钾 | |
| B. | 油脂既能为人体提供热量,又能提供人体必需脂肪酸 | |
| C. | 棉花、羊毛及合成纤维完全燃烧都只生成二氧化碳和水 | |
| D. | 蛋白质遇饱和硫酸铵溶液产生的沉淀能重新溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在NaHS溶液中滴入少量的CuCl2溶液产生黑色沉淀,HS-电离程度增大,反应后溶液pH减小 | |
| B. | 浑浊的苯酚试液中加入饱和Na2CO3溶液变澄清,则酸性:苯酚>碳酸 | |
| C. | 在等浓度NaCl和Na2CrO4稀溶液中滴加AgNO3溶液,先析出AgCl,则Ksp(AgCl)<Ksp(Ag2CrO4) | |
| D. | 等体积、物质的量浓度的HA与NaA(HA为弱酸)混合溶液,其酸碱性取决于Ka(HA)的大小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 复分解反应一定都不属于氧化还原反应 | |
| B. | 在氧化还原反应中,反应物中的金属单质不一定是还原剂 | |
| C. | 在氧化还原反应中,非金属单质不一定是氧化剂 | |
| D. | 置换反应一定都属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铂电极做成网状,可增大与氧气的接触面积 | |
| B. | 该电池通常只需要更换铝板就可继续使用 | |
| C. | 海洋电池中铝板充当负极,发生氧化反应 | |
| D. | 负极反应为:O2+H20+2e-=2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com