
ĪŖĮĖĶź³É½Ģ²ÄÉĻµÄ”°ÖŠŗĶČČµÄ²ā¶Ø”±ÕāøöŹµŃé
£Ø1£©ŹµŃéץÉĻÓŠÉÕ±£Ø“󔢊”Į½øö£©”¢ÅŻÄĖÜĮĻ”¢ÅŻÄĖÜĮĻ°å£ØÖŠŠÄÓŠĮ½øöŠ”æ×£©”¢»·ŠĪ²£Į§½Į°č°ō£¬0.50mol”¤L-1ŃĪĖį”¢0.55mol”¤L”Ŗ1NaOHČÜŅŗ£¬ÉŠČ±ÉŁµÄŹµŃéÓĆĘ·ŹĒ ”£
£Ø2£©ŹµŃéÖŠÄÜ·ńÓĆ»·ŠĪĶĖæ½Į°č°ō“śĢę»·ŠĪ²£Į§½Į°č°ō£æ“š£ŗ £ØĢī”°ÄÜ”±»ņ”°·ń”±£©”£ĘäŌŅņŹĒ ”£
£Ø3£©ŹµŃ鏱ĖłÓĆŃĪĖį¼°NaOHČÜŅŗµÄĢå»ż¾łĪŖ50mL£¬ø÷ČÜŅŗĆܶČĪŖ1g”¤cm”Ŗ3£¬Éś³ÉČÜŅŗµÄ±ČČČČŻc=4.18J/(g”¤”ę)£¬ŹµŃéĘšŹ¼ĪĀ¶ČĪŖt1”ę£¬ÖÕÖ¹ĪĀ¶ČĪŖt2”ę”£ŹŌĶʶĻÖŠŗĶČČµÄ¼ĘĖćŹ½£ŗ ”£
£Ø4£©Čē¹ūÓĆ50mLµÄ0.60mol”¤L-1ŃĪĖįÓė50mL µÄ0.55mol”¤L”Ŗ1NaOHČÜŅŗ½ųŠŠ·“Ó¦”£ČōČČĮæĪŽĖšŹ§£¬ÓėÉĻŹöŹµŃéĻą±Č£¬ĖłĒóÖŠŗĶČČ £ØĢī”°Ę«“ó”¢Ę«Š””¢ĻąµČ”±£©£¬¼ņŹöĄķÓÉ ”£
 ÖĒȤŗ®¼Ł×÷ŅµŌĘÄĻæĘ¼¼³ö°ęÉēĻµĮŠ“š°ø
ÖĒȤŗ®¼Ł×÷ŅµŌĘÄĻæĘ¼¼³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖ450 ”ꏱ£¬·“Ó¦H2(g)£«I2(g) 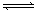 2HI(g)µÄK £½ 50£¬ÓÉ“ĖĶĘ²āŌŚ450 ”ꏱ£¬·“Ó¦2HI(g)
2HI(g)µÄK £½ 50£¬ÓÉ“ĖĶĘ²āŌŚ450 ”ꏱ£¬·“Ó¦2HI(g) 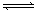 H2(g)£«I2(g)µÄ»ÆŃ§Ę½ŗā³£ŹżĪŖ
H2(g)£«I2(g)µÄ»ÆŃ§Ę½ŗā³£ŹżĪŖ
A”¢50 B”¢0.02 C”¢100 D”¢ĪŽ·ØČ·¶Ø
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚt”ꏱ£¬Ä³NaOHĻ”ČÜŅŗÖŠ£¬c(H+)=10-amol/L£¬c(OH-)=10-bmol/L£¬ŅŃÖŖa+b=12,Ōņ£ŗ
¢ÅøĆĪĀ¶ČĻĀ£¬Ė®µÄĄė×Ó»ż³£ŹżKw= ”£
¢ĘŌŚøĆĪĀ¶ČĻĀ£¬½«100mL0.1mol/LµÄĻ”ĮņĖįÓė100mL0.4mol/LµÄNaOHČÜŅŗ»ģŗĻŗó£¬ČÜŅŗµÄpH= £¬“ĖŹ±øĆČÜŅŗÖŠÓÉĖ®µēĄėµÄc(OH-)= ”£
¢ĒøĆĪĀ¶ČĻĀ£¬Čō100Ģå»żpH1=aµÄijĒæĖįČÜŅŗÓė1Ģå»żpH2=bµÄijĒæ¼īČÜŅŗ»ģŗĻŗóČÜŅŗ³ŹÖŠŠŌ£¬Ōņ»ģŗĻĒ°£¬øĆĒæĖįµÄpH1ÓėĒæ¼īµÄpH2Ö®¼äÓ¦Āś×ćµÄ¹ŲĻµŹĒ ”£
¢ČøĆĪĀ¶ČĻĀ£¬pH=3µÄĮņĖįČÜŅŗŗĶpH=9µÄNaOHČÜŅŗµČĢå»ż»ģŗĻŗ󣬻ģŗĻČÜŅŗµÄpH £ØĢī>7”¢=7”¢<7£©£»pH=3µÄ“×ĖįČÜŅŗŗĶpH=9µÄNaOHČÜŅŗµČĢå»ż»ģŗĻŗ󣬻ģŗĻČÜŅŗµÄpH £ØĢī>7”¢=7”¢<7£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚ1100”ę£¬Ņ»¶ØČŻ»żµÄĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£ŗFeO(s)+CO(g) Fe(s)+CO2(g) ”÷H=a kJ/mol£Øa >0£©£¬øĆĪĀ¶ČĻĀK=0.263£¬ĻĀĮŠÓŠ¹ŲøĆ·“Ó¦µÄĖµ·ØÕżČ·µÄŹĒ
Fe(s)+CO2(g) ”÷H=a kJ/mol£Øa >0£©£¬øĆĪĀ¶ČĻĀK=0.263£¬ĻĀĮŠÓŠ¹ŲøĆ·“Ó¦µÄĖµ·ØÕżČ·µÄŹĒ
A£® ČōÉś³É1 mol Fe£¬ŌņĪüŹÕµÄČČĮæŠ”ÓŚa kJ
B£® ČōÉżøßĪĀ¶Č£¬Õż·“Ó¦ĖŁĀŹ¼Óæģ£¬Äę·“Ó¦ĖŁĀŹ¼õĀż£¬Ōņ»ÆŃ§Ę½ŗāÕżĻņŅʶÆ
C£® ČōČŻĘ÷ÄŚĘųĢåŃ¹Ēæ²»Ėꏱ¼ä±ä»Æ£¬ŌņæÉŅŌÅŠ¶ĻøĆ·“Ó¦ŅŃ“ļµ½»ÆŃ§Ę½ŗāדĢ¬
D£® “ļµ½»ÆŃ§Ę½ŗāדĢ¬Ź±£¬Čōc(CO)=0.100 mol/L£¬Ōņc(CO2)=0.0263 mol/L
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻąĶ¬ĪĀ¶ČĻĀ£¬Ģå»ż¾łĪŖ0.25 LµÄĮ½øöŗćČŻĆܱÕČŻĘ÷ÖŠ·¢ÉśæÉÄę·“Ó¦£ŗ
X2(g) £« 3Y2(g)  2XY3(g) ”÷H£½£92.6 kJ”¤mol£1
2XY3(g) ”÷H£½£92.6 kJ”¤mol£1
ŹµŃé²āµĆ·“Ó¦ŌŚĘšŹ¼”¢“ļµ½Ę½ŗāŹ±µÄÓŠ¹ŲŹż¾ŻČēĻĀ±ķĖłŹ¾£ŗ
| ČŻĘ÷ ±ąŗÅ | ĘšŹ¼Ź±ø÷ĪļÖŹĪļÖŹµÄĮæ/mol | “ļĘ½ŗāŹ±ĢåĻµÄÜĮæµÄ±ä»Æ | ||
| X2 | Y2 | XY3 | ||
| ¢Ł | 1 | 3 | 0 | ·ÅČČ 23.15 kJ |
| ¢Ś | 0.6 | 1.8 | 0.8 | a kJ |
ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ
A£®ČŻĘ÷¢Ł”¢¢ŚÖŠ·“Ó¦µÄĘ½ŗā³£ŹżĻąµČ
B£®ČŻĘ÷¢ŚÖŠ·“Ó¦“ļµ½Ę½ŗāŹ±·Å³öµÄČČĮæĪŖ23.15 kJ
C£®“ļĘ½ŗāŹ±£¬Į½øöČŻĘ÷ÖŠXY3µÄĪļÖŹµÄĮæÅØ¶Č¾łĪŖ2 mol”¤L£1
D£®ČōČŻĘ÷¢ŁĢå»żĪŖ0.20 L£¬Ōņ“ļĘ½ŗāŹ±·Å³öµÄČČĮæ“óÓŚ23.15 kJ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ¹ż³ĢŹōÓŚČĖ¹¤¹ĢµŖµÄŹĒ £Ø £©
A. ŗĻ³É°± B. ÉĮµēŹ± ×Ŗ»ÆĪŖ
×Ŗ»ÆĪŖ
C. ·ÖĄėŅŗĢ¬æÕĘųÖʵŖĘų D. ¶¹æĘ×÷ĪļøłĮö¾ś½«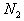 ×Ŗ»ÆĪŖ
×Ŗ»ÆĪŖ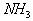
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
øł¾ŻŌ×Ó½į¹¹¼°ŌŖĖŲÖÜĘŚĀɵÄÖŖŹ¶£¬ĻĀĮŠĶʶĻÕżČ·µÄŹĒ £Ø £©
A£®Ķ¬Ö÷×åŌŖĖŲŗ¬ŃõĖįµÄĖįŠŌĖęŗĖµēŗÉŹżµÄŌö¼Ó¶ų¼õČõ
B£®ŗĖĶāµē×ÓÅŲ¼ĻąĶ¬µÄĪ¢Į£»ÆѧŠŌÖŹŅ²ĻąĶ¬
C£®Cl‾”¢S2‾”¢Ca2+”¢K+°ė¾¶Öš½„¼õŠ”
D£®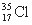 Óė
Óė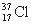 µĆµē×ÓÄÜĮ¦ĻąĶ¬
µĆµē×ÓÄÜĮ¦ĻąĶ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijŠ©»Æѧ·“Ó¦æÉÓĆĻĀŹ½±ķŹ¾£ŗ A + B ”ś C+ D + H2O ”£ Ēė»Ų“šĻĀĮŠĪŹĢā£Ø·“Ó¦æÉŅŌŹĒ¹ĢĢåÖ®¼äµÄ·“Ó¦£¬Ņ²æÉŅŌŹĒŌŚĖ®ČÜŅŗÖŠ½ųŠŠµÄ·“Ó¦£©£ŗ
£Ø1£©ČōCŹĒŅ»ÖÖ¼īŠŌĘųĢ壬³£ÓĆ×÷ÖĘĄä¼Į”£ŌņCĪŖ £ØĢī»ÆѧŹ½ĻĀĶ¬£©”£ŹµŃéŹŅÖĘČ”CĘųĢåµÄ»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø2£©ČōAĪŖ·Ē½šŹō¹ĢĢ¬µ„ÖŹ£¬C”¢D¾łĪŖĘųĢåĒŅ¶¼ÄÜŹ¹³ĪĒåŹÆ»ŅĖ®±ä»ė×ĒĒŅCÄÜŹ¹äåĖ®ĶŹÉ«”£ŌņAĪŖ ”£Š“³öCÓėäåĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½ ”£
£Ø3£© ČōAĪŖ×ĻŗģÉ«½šŹō£¬DĪŖŗģ×ŲÉ«ĘųĢ唣ŌņAĪŖ ”£DÓėĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
øł¾ŻĻĀĮŠŹĀŹµ£ŗ¢ŁX£«Y2+£½X2+£«Y£»¢ŚZ£«H2O£ØĄä£©£½Z(OH)2£«H2”ü£»¢ŪZ2+Ńõ»ÆŠŌ±ČX2+Čõ£»¢ÜÓÉY”¢Wµē¼«×é³ÉµÄµē³Ų£¬µē¼«·“Ó¦ĪŖW2+£«2e-£½W”¢Y£2e-£½Y2+£¬æÉÖŖX”¢Y”¢Z”¢WµÄ»¹ŌŠŌÓÉĒæµ½ČõµÄĖ³ŠņĪŖ
A. X > Z > Y > W B. Z > W > X > Y
C. Z > Y > X > W D. Z > X > Y > W
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com