
汽车尾气(含烃类、CO、NO与SO2等)是城市主要污染源之一,治理的办法之一是在汽车排气管上装催化转化器,它使NO与CO反应生成可参与大气生态循环的无毒气体,反应原理:2NO(g)+2CO(g)===N2(g)+2CO2(g),在298 K、101 kPa下,ΔH=-113 kJ·mol-1、ΔS=-145 J·mol-1·K-1。下列说法中错误的是( )
A.该反应中反应物的总能量高于生成物的总能量
B.该反应常温下不能自发进行,因此需要高温和催化剂
C.该反应常温下能自发进行,高温和催化剂只是加快反应的速率
D.汽车尾气中的这两种气体会与血红蛋白结合而使人中毒
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
常温下,下列有关电解质溶液的叙述正确的是 ( )
A.等浓度等体积的强酸与强碱溶液混合后,溶液的pH=7
B.pH=2的盐酸与pH=12的氨水等体积混合后所得溶液显中性
C.pH=10的Ba(OH)2溶液和pH=13的NaOH溶液等体积混合后溶液的pH=10.7(已知lg 2=0.3)
D.将10 mL pH=a的盐酸与100 mL pH=b的Ba(OH)2溶液混合后恰好中和,则a+b=13
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数依次增大的X、Y、Z、R、W、T六种前20号元素,X、Y原子的最外层电子数与其电子层数相等,Y、T位于同族,R最外层电子数是次外层的3倍,W无正价,甲的化学式为ZX3,是一种刺激性气味的气体,乙是由X、Z、W组成的盐。下列说法正确的是
A.由X、Z、W组成盐的水溶液呈酸性,则溶液中该盐阳离子浓度小于酸根离子浓度
B.气态氢化物的稳定性:W<R< Z
C.原子半径:W <Z<Y,而简单离子半径:Y<Z<W
D.ZR2、TR2两化合物中R的化合价相同
查看答案和解析>>
科目:高中化学 来源: 题型:
盐酸利多卡因(F)葡萄糖注射液抗心律失常,可用于急性心肌梗死后室性早搏和室性心动过速。合成路线如下:
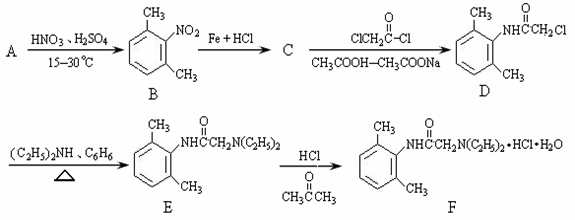
(1)B在核磁共振氢谱上有 种特征峰,D→E的反应类型是 。(每空2分)
(2)C的结构简式为 。(2分)
(3)写出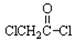 与足量的NaOH溶液共热充分反应的化学方程式:(3分)
与足量的NaOH溶液共热充分反应的化学方程式:(3分)
。
(4)B的同分异构体种类很多,符合以下条件的B的同分异构体共有 种。(3分)
①属于苯的衍生物,苯环上共有三个取代基;
②与碳酸钠溶液反应可放出CO2气体。
查看答案和解析>>
科目:高中化学 来源: 题型:
以下自发反应可用能量判据来解释的是( )
A.硝酸铵自发地溶于水
B.2N2O5(g)===4NO2(g)+O2(g)
ΔH=56.7 kJ·mol-1
C.(NH4)2CO3(s)===NH4HCO3(s)+NH3(g)
ΔH=74.9 kJ·mol-1
D.2H2(g)+O2(g)===2H2O(l)
ΔH=-285.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应概念正误判断,正确的打“√”,错误的打“×”
(1)有化合价升降的化学反应一定是氧化还原反应( )
(2)置换反应全部属于氧化还原反应,因为有单质参加和生成,化合价发生了变化( )
(3)氧化还原反应一定属于四大基本反应类型( )
(4)有单质参加或生成的化学反应一定是氧化还原反应( )
(5)氧化还原反应中,反应物不是氧化剂就是还原剂( )
(6)在氧化还原反应中,氧化剂和还原剂既可以是不同物质也可以是同种物质( )
(7)在氧化还原反应中,非金属单质都做氧化剂( )
(8)生成物中来源于氧化剂的是还原产物( )
(9)还原剂具有还原性,反应时本身被还原,发生还原反应( )
(10)元素从化合态变为游离态,该元素不一定被还原( )
(11)失电子越多,还原性越强,得电子越多,氧化性越强( )
(12)在同一氧化还原反应中,氧化剂的氧化性一定大于氧化产物的氧化性( )
(13)金属元素被还原,不一定得到金属单质( )
(14)含氧酸的价态越高,氧化性一定越强( )
(15)不容易得到电子的物质,肯定容易失去电子( )
查看答案和解析>>
科目:高中化学 来源: 题型:
下列变化按氮元素只被氧化、只被还原、既不被氧化又不被还原、既可能被氧化又可能被还原的顺序排列正确的是( )
①高能固氮 ②硝酸分解 ③实验室制取氨气 ④氨氮废水脱氮(指将NH3或NH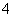 转化为N2)
转化为N2)
A.④②③① B.②①③④
C.③④②① D.③①④②
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌[含有Fe(Ⅱ)、Mn(Ⅱ)、Ni(Ⅱ)等杂质]的流程如下:
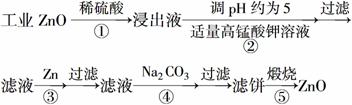
提示:在本实验条件下,Ni(Ⅱ)不能被氧化;高锰酸钾的还原产物是MnO2。
则:反应②中除掉的杂质离子是__________,发生反应的离子方程式为__________;在加高锰酸钾溶液前,若pH较低,对除杂的影响是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,改变反应物的用量或浓度,不会改变反应产物种类的是( )
A.炭粉在氧气中燃烧
B.CO2通入氢氧化钠溶液
C.铁在氯气中燃烧
D.铜和硝酸反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com