
| A. | 质子数和中子数 | B. | 中子数和电子数 | ||
| C. | 核电荷数和电子数 | D. | 质量数和电子数 |
分析 微粒的结构示意图是表示微粒的核电荷数和电子层排布的图示形式,而中子数和质量数没有体现,据此进行判断.
解答 解:A.在微粒的原子结构示意图上,只能体现出原子核电荷数和电子层排布的图示形式,中子数没有体现,故A错误;
B.在微粒的原子结构示意图上,只能体现出原子核电荷数和电子层排布的图示形式,中子数没有体现,故B错误;
C.微粒结构示意图是表示原子核电荷数和电子层排布的图示形式,能反映出核电荷数和核外电子层排布的情况,即能反应出核电荷数和电子数,故C正确;
D.在微粒的原子结构示意图上,只能体现出原子核电荷数和电子层排布的图示形式,质量数数没有体现,故D错误;
故选C.
点评 本题考查了原子结构示意图表示的意义,题目难度不大,明确原子结构示意图的表示方法为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:解答题

| 温度/℃ | 400 | 500 | 600 |
| SO2转化率/% | 99.2 | 93.5 | 73.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
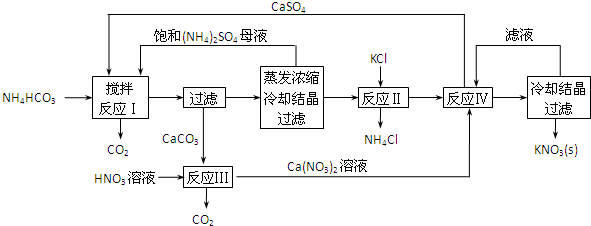
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
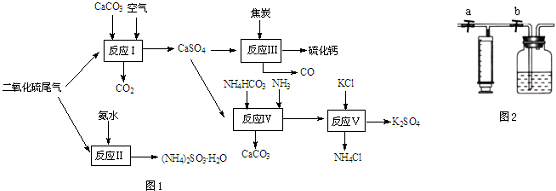
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠溶液与盐酸反应:Na2CO3+2H+═2Na++H2O+CO2↑ | |
| B. | 氧化铜与硫酸溶液反应:Cu2++2H+═Cu2++H2O | |
| C. | 锌与稀硫酸反应:Zn+2H+═Zn2++H2↑ | |
| D. | 硫酸铜溶液中放入铁片:3Cu2++2Fe═2Fe3++3Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⅠA族元素的金属性比ⅡA族元素的金属性强 | |
| B. | 第三周期元素的离子半径从左到右逐渐减小 | |
| C. | 同周期非金属氧化物对应的水化物的酸性从左到右依次增强 | |
| D. | ⅣA族元素的氢化物中,稳定性最好的是CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
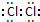 ;
;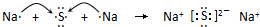 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 锌片溶解了32.5 g | B. | 锌片增重32.5 g | ||
| C. | 铜片上析出lgH2 | D. | 铜片上析出1molH2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com