
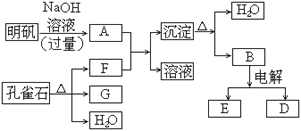
【题目】在一定条件下可实现下图所示物质之间的变化:
请填写以下空白:
(1)孔雀石的主要成分是CuCO3·Cu(OH)2(碱式碳酸铜),受热易分解。下图中的F是_____。
(2)写出明矾溶液与过量NaOH溶液反应的离子方程式:________。
(3)图中所得G和D都为固体,混和后在高温下可发生反应,写出该反应的化学方程式:____________。
(4)每生成1摩D,同时生成______摩E。
【答案】CO2(或二氧化碳) Al3++4OH-=[Al(OH)4]- 3CuO+2Al= Al2O3+ 3Cu ![]()
【解析】
根据不活泼金属碳酸盐受热易分解成金属氧化物和CO2,以及不活泼金属的氢氧化物受热易分解成金属氧化物和H2O的规律,可推知孔雀石的分解产物为CuO、CO2和H2O,由题意知G为固体即CuO,则F为气体CO2。根据明矾的组成以及Al3+的性质可知A为含有NaAlO2的溶液,B为氢氧化铝受热分解的产物之一,为Al2O3,根据电解冶炼铝可以得到金属铝,推知D为Al,E为O2,用Al作还原剂可以还原CuO,据此分析作答。
(1)由以上分析可知F为CO2,为共价化合物;
(2)明矾溶液与过量NaOH溶液反应的实质是:铝离子和氢氧根之间的反应,离子方程式为:Al3++4OH-=[Al(OH)4]-;
(3)G为氧化铜,B为氢氧化铝受热分解的产物之一,为氧化铝,电解产物为铝,铝和氧化铜高温下的反应为:3CuO+2Al= Al2O3+ 3Cu;
(4)氧化铝电解的反应为:2Al2O3![]() 4Al+3O2↑,属于氧化还原反应,图中所得G和D都为固体,所以D为铝,每生成1摩铝,同时生成3/4 mol的氧气。
4Al+3O2↑,属于氧化还原反应,图中所得G和D都为固体,所以D为铝,每生成1摩铝,同时生成3/4 mol的氧气。


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
【题目】雾霾由多种污染物形成,包含颗粒物(PM2.5)、氮氧化物(NOx)、CO、SO2等。化学在解决雾霾污染问题中有着重要的作用。
(1)已知:①2CO(g)+O2(g)=2CO2(g)△H1=-566.0kJ·mol-1
②N2(g)+2O2(g)=2NO2(g)△H2=+64kJ·mol-1
反应2NO2(g)+4CO(g=N2(g)+4CO2(g)在__________(填“高温”或“低温”)条件下能自发进行。
(2)研究发现利用NH3可除去硝酸工业尾气中的NO。NH3与NO的物质的量之比分别为1:2、1:1.5、3:1时,NO脱除率随温度变化的曲线如图1所示。
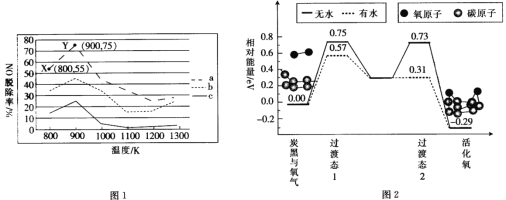
①曲线a中,NO的起始浓度为6×10-4mg·m-3,若从X点到Y点经过20s,则该时间段内NO的脱除速率为_________mg·m-3·s-1。
②曲线c对应的NH3与NO的物质的量之比是________,其理由是__________
(3)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化氧可以快速氧化SO2。活化过程中的能量变化模拟计算结果如图2所示。无水情况下,一个氧分子的活化能为__________,容易活化氧分子的条件是_________(填“有水”或“无水”)。
(4)若反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g)的正、逆反应速率分别可表示为v正=k正c2(NO)·c2(CO);v逆=k逆c(N2)·c2(CO2),k正、k逆分别为正、逆反应速率常数,c为物质的量浓度。一定温度下,在体积为1L的恒容密闭容器中加入4molNO和4molCO发生上述反应,测得CO和CO2的物质的量浓度随时间的变化如图3所示。
N2(g)+2CO2(g)的正、逆反应速率分别可表示为v正=k正c2(NO)·c2(CO);v逆=k逆c(N2)·c2(CO2),k正、k逆分别为正、逆反应速率常数,c为物质的量浓度。一定温度下,在体积为1L的恒容密闭容器中加入4molNO和4molCO发生上述反应,测得CO和CO2的物质的量浓度随时间的变化如图3所示。
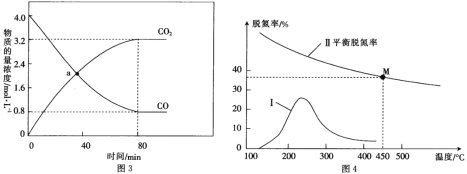
①a点时,v逆:v正=_____________。
②测得平衡时体系压强为p,KP为用气体分压表示的平衡常数,分压=总压×物质的量分数,则平衡常数KP=____________(用含p的式子表示)。
(5)某研究小组探究该反应中催化剂对脱氮率(NO的转化率)的影响。将等物质的量的NO和CO以一定的流速分别通过催化剂a、b,发生反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。相同时间、不同温度下测得使用催化剂a时脱氮率与温度的关系如图4中曲线Ⅰ所示。已知催化效率b>a,催化剂b的活性在450℃时最大(未达平衡)。请在图4中画出使用催化剂b时所对应的曲线(从300℃开始画)。_______________
N2(g)+2CO2(g)。相同时间、不同温度下测得使用催化剂a时脱氮率与温度的关系如图4中曲线Ⅰ所示。已知催化效率b>a,催化剂b的活性在450℃时最大(未达平衡)。请在图4中画出使用催化剂b时所对应的曲线(从300℃开始画)。_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.一定温度下,反应MgCl2(l)=Mg(1)+Cl2(g)的 △H>0 △S>0
B.用N2(g)+3H2(g)=2NH3(g)△H<0设计的燃料电池,N2(g)在正极上进行反应
C.氯化镁溶液加热蒸干得不到纯净氯化镁固体
D.常温下,向饱和![]() 溶液中加少量
溶液中加少量![]() 粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,说明常温下
粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,说明常温下![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯氯乙酮是一种具有荷花香味且有强催泪作用的杀伤性化学毒剂,它的结构简式如图所示,下列说法错误的是
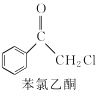
A.分子式为C8H7OClB.在同一平面上的碳原子最多有8个
C.1mol苯氯乙酮最多可与3molH2发生加成反应D.核磁共振氢谱有4个吸收峰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B分别为第三周期和第四周期的同一主族不同元素的原子,它们原子核内的质子数都等于中子数,①若A为ⅢA族,其质量数为x,则B的质子数为y;②若A为ⅡA族,其质子数为m,则B的质量数为n,在下列各组值中,y和n的值分别是
A.(![]() +18)和(2m+16)B.(
+18)和(2m+16)B.(![]() +8)和(2m+16)
+8)和(2m+16)
C.(![]() +8)和(2m+36)D.(
+8)和(2m+36)D.(![]() +18)和(2m+36)
+18)和(2m+36)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某微粒A的结构示意图为![]()
(1)若A是原子,则A的元素符号为__;若A是带一个正电荷的阳离子,则X=___
(2)若X=8,则此阴离子与(1)中带一个正电荷的阳离子形成一种常见化合物的化学式是___,它是不是电解质(填是或否)____。写出此化合物与盐酸反应的化学方程式:________________________________
(3)1mol微粒A含有10mol电子,下列微粒各1mol,也含有10mol电子的有:___(填序号)
①CH4 ②H2O2 ③HF ④Al3+ ⑤Cl- ⑥NH4+
(4)若A的阳离子为An+且质量数为a,则其质子数为____________,中子数为_______________(用含有a,n的代数式表达)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X与Y可形成化合物![]() ,2元素可形成负一价离子。下列说法正确的是( )
,2元素可形成负一价离子。下列说法正确的是( )
A.X元素基态原子的电子排布式为![]()
B.X元素是第4周期第VA族元素
C.Y元素原子的轨道表示式为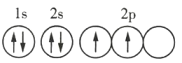
D.Z元素的单质Z2在氧气中不能燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次递增的短周期元素W、X、Y、Z组成的化合物a、b、c、d、e、f,其中b、c与人的呼吸活动息息相关,m为单质,它们的转化关系如图所示。下列叙述不正确的是

A.原子半径:W<Y<X<Z
B.由W、X、Y、Z构成的化合物中可能含有离子键、极性共价键和非极性共价键
C.X的氢化物沸点可能比Y的氢化物沸点高
D.Z2Y2中阴阳离子个数比为1:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com