
·ÖĪö £Ø1£©ÓŠA”¢B”¢C”¢DĖÄÖÖĒæµē½āÖŹ£¬ĖüĆĒŌŚĖ®ÖŠµēĄėŹ±æɲśÉśĻĀĮŠĄė×Ó£ØĆæÖÖĪļÖŹÖ»ŗ¬ÓŠŅ»ÖÖŅõĄė×ÓĒŅ»„²»ÖŲø“£©£¬
¢ŁA”¢CČÜŅŗpH¾ł“óÓŚ7£¬ĖµĆ÷Ņ»ÖÖŹĒĒæ¼ī£¬Ņ»ÖÖŹĒČõĖįĒæ¼īŃĪ£¬ČõĖįĒæ¼īŃĪŹĒ“×ĖįÄĘ£»
¢ŚCČÜŅŗŗĶDČÜŅŗĻąÓöֻɜ³É°×É«³Įµķ£¬ĖµĆ÷Ņ»ÖÖČÜŅŗŗ¬ÓŠ±µĄė×Ó£¬Ņ»ÖÖČÜŅŗŗ¬ÓŠĮņĖįøłĄė×Ó£»
BČÜŅŗŗĶCČÜŅŗĻąÓöŹ±Ö»Éś³É“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢ壬ĖµĆ÷Ņ»ÖÖČÜŅŗŗ¬ÓŠļ§øłĄė×Ó£¬Ņ»ÖÖČÜŅŗŗ¬ÓŠĒāŃõøłĄė×Ó£¬AČÜŅŗŗĶDČÜŅŗ»ģŗĻŹ±ĪŽĆ÷ĻŌĻÖĻó£¬ĒŅĻąĶ¬ÅØ¶ČµÄA”¢BµÄČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶ČĻąĶ¬£¬ĖłŅŌAŹĒ“×ĖįÄĘ”¢BŹĒĀČ»Æļ§”¢CŹĒĒāŃõ»Æ±µ”¢DŹĒĮņĖįÄĘ£¬¾Ż“Ė·ÖĪö£»
£Ø2£©øł¾ŻČÜŅŗÖŠµēŗÉŹŲŗć”¢ĪļĮĻŹŲŗć¼ĘĖćc£ØH+£©-c£ØNH3•H2O£©£»
£Ø3£©øł¾ŻĢāŅāÖŖ£¬ĀČ»Æļ§ŗĶĒāŃõ»Æ±µµÄĪļÖŹµÄĮæĻąµČ£¬»ģŗĻŗó£¬ČÜŅŗÖŠµÄČÜÖŹŹĒ°±Ė®”¢ĀČ»Æ±µŗĶĒāŃõ»Æ±µ£¬ĀČ»Æ±µŗĶĒāŃõ»Æ±µµÄÅضČĻąµČ£¬°±Ė®µÄÅØ¶ČŹĒĀČ»Æ±µŗĶĒāŃõ»Æ±µÅØ¶ČµÄ2±¶£¬øł¾ŻČÜŅŗÖŠµÄČÜÖŹŠŌÖŹČ·¶ØĄė×ÓÅØ¶Č¹ŲĻµ£»
£Ø4£©»ģŗĻČÜŅŗµÄpH=11£¬ŌņČÜŅŗÖŠĒāŃõøłĄė×ÓÅضČ=$\frac{1{0}^{-14}}{1{0}^{-11}}$=10-3 mol/L£¬øł¾Żc£ØOH-£©=$\frac{n£ØO{H}^{-}£©-n£Ø{H}^{+}£©}{»ģŗĻČÜŅŗĢå»ż}$¼ĘĖćĒāŃõ»Æ±µŗĶŃĪĖįµÄĢå»żÖ®±Č£®
½ā“š ½ā£ŗ¢ŁA”¢CČÜŅŗµÄpH¾ł“óÓŚ7£¬Ó¦ĪŖ“×ĖįŃĪŗĶ¼īČÜŅŗ£¬A”¢BµÄČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶ČĻąĶ¬£¬ŌņČÜŅŗĖ®½ā³Ģ¶ČĻąĶ¬£»
¢ŚCČÜŅŗŗĶDČÜŅŗĻąÓöŹ±Ö»Éś³É°×É«³Įµķ£¬BČÜŅŗŗĶCČÜŅŗĻąÓöŹ±Ö»Éś³É“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢ壬AČÜŅŗŗĶDČÜŅŗ»ģŗĻŹ±ĪŽĆ÷ĻŌĻÖĻó£¬ŌņĖµĆ÷CĪŖBa£ØOH£©2£¬DĪŖNa2SO4£¬ŌņBĪŖNH4Cl£¬AĪŖCH3COONa£¬
£Ø1£©øł¾ŻĢāÖŠŠÅĻ¢ĶʶĻ³öø÷ĪļÖŹ·Ö±šĪŖ£ŗAĪŖCH3COONa£¬BĪŖNH4Cl£¬CĪŖBa£ØOH£©2£¬DĪŖNa2SO4£¬
¹Ź“š°øĪŖ£ŗCH3COONa£»Na2SO4£»
£Ø2£©øł¾ŻČÜŅŗÖŠµēŗÉŹŲŗćµĆc£ØH+£©+c£ØNH4+£©=c£ØOH-£©+c£ØCl-£©£¬øł¾ŻČÜŅŗÖŠĪļĮĻŹŲŗćµĆ c£ØNH3£®H2O£©+c£ØNH4+£©=c£ØCl-£©£¬½«Į½øöµČŹ½Ļą¼õµĆc£ØH+£©-c£ØNH3•H2O£©=c£ØOH-£©=1”Į10£Øx-14£©£¬¹Ź“š°øĪŖ£ŗ1”Į10£Øx-14£©£»
£Ø3£©øł¾ŻĢāŅāÖŖ£¬ĀČ»Æļ§ŗĶĒāŃõ»Æ±µµÄĪļÖŹµÄĮæĻąµČ£¬»ģŗĻŗó£¬ČÜŅŗÖŠµÄČÜÖŹŹĒ°±Ė®”¢ĀČ»Æ±µŗĶĒāŃõ»Æ±µ£¬ĀČ»Æ±µŗĶĒāŃõ»Æ±µµÄÅضČĻąµČ£¬°±Ė®µÄÅØ¶ČŹĒĀČ»Æ±µŗĶĒāŃõ»Æ±µÅØ¶ČµÄ2±¶£¬ČÜŅŗÖŠĒāŃõøłĄė×ÓÅضČ×ī“󣬱µĄė×ÓŗĶĀČĄė×ÓÅضČĻąµČ£¬°±Ė®ŹĒČõ¼ī²æ·ÖµēĄėµ¼ÖĀĀČĄė×ÓÅØ¶Č“óÓŚļ§øłĄė×ÓÅØ¶Č£¬ČÜŅŗ³Ź¼īŠŌ£¬ĒāĄė×ÓÅضČ×īŠ”£¬ĖłŅŌČÜŅŗÖŠĄė×ÓÅØ¶Č“óŠ”Ė³ŠņŹĒc£ØOH-£©£¾c£ØBa2+£©=c£ØCl-£©£¾c£ØNH4+£©£¾c£ØH+£©£¬
¹Ź“š°øĪŖ£ŗc£ØOH-£©£¾c£ØBa2+£©=c£ØCl-£©£¾c£ØNH4+£©£¾c£ØH+£©£»
£Ø4£©»ģŗĻČÜŅŗµÄpH=11£¬ŌņČÜŅŗÖŠĒāŃõøłĄė×ÓÅضČ=$\frac{1{0}^{-14}}{1{0}^{-11}}$=10-3 mol/L£¬ÉčĒāŃõ»Æ±µµÄĢå»żĪŖX£¬ŃĪĖįµÄĢå»żĪŖY£¬c£ØOH-£©=$\frac{n£ØO{H}^{-}£©-n£Ø{H}^{+}£©}{»ģŗĻČÜŅŗĢå»ż}$=$\frac{0.005”Į2”ĮX-0.00125Y}{X+Y}$=10-3 mol/L£¬X£ŗY=1£ŗ4£¬¹Ź“š°øĪŖ£ŗ1£ŗ4£®
µćĘĄ ±¾ĢāŅŌ»ÆŗĻĪļµÄĶʶĻĪŖŌŲĢåæ¼²éĮĖĪļÖŹµÄĮæµÄÓŠ¹Ų¼ĘĖć”¢Ąė×ÓÅØ¶Č“óŠ”µÄ±Č½ĻµČÖŖŹ¶µć£¬Ć÷Č·ĪļÖŹµÄŠŌÖŹŹĒĶʶĻ»ÆŗĻĪļµÄ¹Ų¼ü£¬±¾ĢāµÄÄѵćŹĒÅŠ¶ĻČÜŅŗÖŠĄė×ÓÅØ¶Č“óŠ”µÄ±Č½Ļ£¬øł¾ŻĪļĮĻŹŲŗćŗĶµēŗÉŹŲŗćĄ“ÅŠ¶Ļ¼“æÉ£¬Äѵć½Ļ“ó£®


 ÖĒÄÜѵĮ·Į·²āæ¼ĻµĮŠ“š°ø
ÖĒÄÜѵĮ·Į·²āæ¼ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Si”¢P”¢SŌŖĖŲµÄ×īøßÕż¼ŪŅĄ“Ī½µµĶ | |
| B£® | Li”¢Na”¢KµÄŌ×Ó°ė¾¶ŅĄ“ĪŌö“ó | |
| C£® | C”¢O”¢NµÄŌ×Ó°ė¾¶ŅĄ“Ī¼õŠ” | |
| D£® | Na”¢Mg”¢AlŌ×ÓµÄ×īĶā²ćµē×ÓŹżŅĄ“Ī¼õÉŁ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĶÖ¬”¢ĢĒĄąŗĶµ°°×ÖŹŹĒČż“óÓŖŃųĪļÖŹ£¬¶¼ÄÜ·¢ÉśĖ®½ā£»±»³Ę×÷”°ČĖĢåŗĖĪäĘ÷”±µÄĪ¬ÉśĖŲB2ŗ¬ÓŠėļü½į¹¹µČ£¬Ņ²ÄÜ·¢ÉśĖ®½ā | |
| B£® | 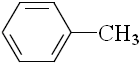 ”¢ ”¢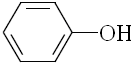 ŗĶ ŗĶ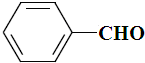 £¬½öµŚŅ»ÖÖÄÜŹ¹KMnO4ĖįŠŌČÜŅŗĶŹÉ« £¬½öµŚŅ»ÖÖÄÜŹ¹KMnO4ĖįŠŌČÜŅŗĶŹÉ« | |
| C£® | °±»łĖįÖ÷ŅŖŅŌÄŚŃĪŠĪŹ½“ęŌŚ£¬µ÷½ŚČÜŅŗµÄpH²»æÉøıäĖüŌŚĖ®ÖŠµÄČܽā¶Č | |
| D£® | Ģå¼ģ±Øø굄֊µÄ”°øŹÓĶČżõ„”±ŹĒøŹÓĶµÄŃÜÉśĪļ£¬ĘäÖŠøŹÓĶ½į¹¹¼ņŹ½ŹĒ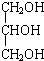 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆŹ³“׳żČ„ČČĖ®ĘæÖŠµÄĖ®¹ø£ŗCO32-+2CH3COOHØT2CH3COO-+CO2”ü+H2O | |
| B£® | AlČÜÓŚNaOHČÜŅŗ£ŗAl+2OH-ØTAlO2-+H2”ü | |
| C£® | Cl2ČÜÓŚĖ®£ŗCl2+H2OØTH++Cl-+HClO | |
| D£® | NaHSO4ČÜŅŗÓėBa£ØOH£©2ČÜŅŗ·“Ó¦ÖĮÖŠŠŌ£ŗH++SO42-+Ba2++OH-ØTBaSO4”ż+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 3.9gNa2O2¾§ĢåÖŠŅõŃōĄė×Ó×ÜŹżĪŖ0.15NA | |
| B£® | 1.0L1.0mo1•L-1µÄNaNO3Ė®ČÜŅŗÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżĪŖ3NA | |
| C£® | 25”ꏱpH=13µÄBa£ØOH£©2ČÜŅŗÖŠŗ¬ÓŠOHŅ»µÄŹżÄæĪŖ0.1NA | |
| D£® | 1 molµÄōĒ»łÓė1 molµÄĒāŃõøłĄė×ÓĖłŗ¬µē×ÓŹż¾łĪŖ9NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
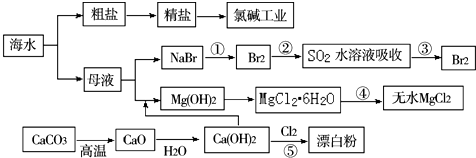
| A£® | Cl2”¢ĘÆ°×·ŪŗĶSO2¾łæÉŅŌĘÆ°×ÓŠÉ«ĪļÖŹ£¬ĒŅĘÆ°×µÄŌĄķĻąĶ¬ | |
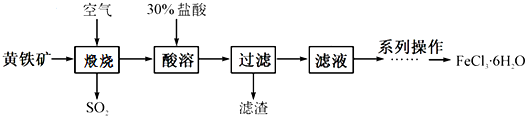
| B£® | ĀČ¼ī¹¤Ņµ¾ĶŹĒÖø¹¤ŅµÉĻµē½ā±„ŗĶŹ³ŃĪĖ®µÄ·½·ØÖĘČ”NaOH”¢Cl2”¢H2µÄ¹ż³Ģ | |
| C£® | ¹¤¶Ī¢Ü±ŲŠėŌŚøÉŌļµÄHClĘųĮ÷ÖŠ¼ÓČČ²ÅÄÜÖĘČ”ĪŽĖ®MgCl2 | |
| D£® | ¹¤¶Ī¢Ł¢Ś¢Ū·¢ÉśµÄ·“Ó¦¾łĪŖŃõ»Æ»¹Ō·“Ó¦£¬ĒŅäåŌŖĖŲ¾ł±»Ńõ»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
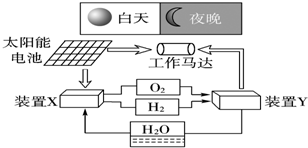
| A£® | ¶žŃõ»Æ¹čŹĒĢ«ŃōÄܵē³ŲµÄ¹āµē×Ŗ»»²ÄĮĻ | |
| B£® | ×°ÖĆXÄÜŹµĻÖČ¼ĮĻµē³ŲµÄĒāĘųŗĶŃõĘųŌŁÉś | |
| C£® | ×°ÖĆYÖŠøŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗO2+2H2O+4e-ØT4OH- | |
| D£® | ×°ÖĆX”¢YŠĪ³ÉµÄ×ÓĻµĶ³ÄÜŹµĻÖĪļÖŹµÄĮćÅÅ·Å£¬²¢ÄÜŹµĻÖ»ÆѧÄÜÓėµēÄܼäµÄĶźČ«×Ŗ»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼×ŅŅĮ½·Ż»ģŗĻĪļÖŠ¾łŗ¬Na2O20.16mol | |
| B£® | ¼×ŅŅĮ½·Ż»ģŗĻĪļÖŠ¾łŗ¬NaHCO30.02mol | |
| C£® | Ō»ģŗĻĪļÖŠNa2O2ÓėNaHCO3ĪļÖŹµÄĮæÖ®±ČĪŽ·ØČ·¶Ø | |
| D£® | ŃĪĖįĪļÖŹµÄĮæÅضČæÉÄÜĪŖ3.4mol/L |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com