
| A、1个 | B、2个 | C、3个 | D、4个 |


科目:高中化学 来源: 题型:
| A、NaOH |
| B、KI |
| C、AgNO3 |
| D、FeCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
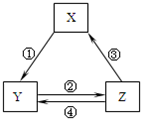 下表各组物质之间通过一步反应不可以实现如右图所示转化关系的是( )
下表各组物质之间通过一步反应不可以实现如右图所示转化关系的是( )| 选项 | X | Y | Z | 箭头上所标 数字的反应条件 |
| A | SiO2 | Na2SiO3 | H2SiO3 | ①与Na2CO3熔融 |
| B | NaCl | NaHCO3 | Na2CO3 | ②加热 |
| C | N2 | NO2 | HNO3 | ③加热 |
| D | C | CO | CO2 | ④灼热炭粉 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向FeSO4溶液中滴加硫氰化钾溶液,溶液呈血红色,说明FeSO4溶液未变质 |
| B、铅蓄电池放电时的负极和充电时的阴极均发生氧化反应 |
| C、反应2Mg(s)+CO2(g)=C(s)+2MgO(s)能自发进行,则该反应的△H<0 |
| D、物质的量浓度相等的下列物质溶液中,c(NH4+)大小顺序为:NH4HCO3>NH4NO3>NH4Fe(SO4)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、abc | B、bcd |
| C、cba | D、abcd |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由H2、I2蒸气、HI组成的平衡体系加压后颜色变深 |
| B、500℃时比室温更有利于合成氨的反应 |
| C、合成氨工厂通常采用较高压强,以提高原料的利用率 |
| D、合成氨工业中用铁触媒做催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| A、平衡前,随着反应的进行,容器内压强始终不变 |
| B、当v(SO 2 )顺=2v(CO2)逆时,反应达到平衡状态 |
| C、平衡时,其他条件不变,升高温度可提高SO2的转化率 |
| D、平衡后,充入CO、CO2气体,使CO和CO2浓度均为原来的两倍,平衡不移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com