
下列叙述正确的是( )
A.1个甘氨酸分子中存在9对共用电子
B.PCl3和了BCl3分子中所有原子的最外层都达到8电子稳定结构
C.H2S和CS2分子都是含极性键的极性分子
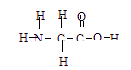 D.熔点由高到低的顺序是:金刚石>碳化硅>晶体硅
D.熔点由高到低的顺序是:金刚石>碳化硅>晶体硅
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com