
| A.常温下反应2M2+ + Z2 ="=" 2M3+ + 2Z-可以自发进行 |
| B.Z元素在反应①中被氧化,在③中被还原 |
| C.氧化性强弱顺序为: XO4- < Z2 < R2 < M3+ |
| D.还原性强弱顺序为: X2+ < Z- < R- < M2+ |


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源:不详 题型:单选题
A.2Fe3++SO2+2H2O = 2Fe2++SO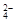 +4H+ +4H+ | B.I2+SO2+2H2O = H2SO4+2HI |
| C.H2O2+H2SO4 = SO2↑+O2↑+2H2O | D.2Fe2++Cl2 = 2Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2S>H2SO3>I—>Br— | B.Br—>I—>H2SO3>H2S |
| C.H2SO3>H2S>Br—>I— | D.I—>Br—>H2S>H2SO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应Z2+2A2+====2A3++2Z-可以进行 | B.Z元素在①③反应中均被还原 |
| C.氧化性强到弱的顺序是XO4->Z2>B2>A3+ | D.还原性由强到弱的顺序是A2+>B->Z->X2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
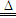 3HCNO; ② 8HCNO+6NO2
3HCNO; ② 8HCNO+6NO2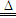 7N2+8CO2+4H2O
7N2+8CO2+4H2O| A.反应①中的两种物质互为同素异形体 | B.反应②中HCNO是氧化剂 |
| C.反应②中NO2是还原剂 | D.反应②中转移的电子数为24 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.Na2O2 +2HCl= 2NaCl+H2O2 | B.Ag2O+ H2O2=2Ag+O2+ H2O |
| C.2 H2O2="2" H2O+O2 | D.3 H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8 H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.FeCl3 > Cl2 > I2 | B.Cl2 > FeCl3 > I2 | C.I2> Cl2 > FeCl3 | D.Cl2> I2> FeCl3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com