
【题目】(1)向密度为1.45 g·cm-3的硫酸溶液中,逐滴加入氯化钡溶液直至沉淀完全。过滤后所得溶液质量与加入的氯化钡溶液质量相等。则原硫酸溶液的物质的量浓度是_______。
(2)在1.00 L 1.00 mol·L-1的NaOH溶液中通过16.8 L(标准状况)CO2,计算所得溶液中含有NaHCO3和Na2CO3的物质的量________和____________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如图所示,ΔH1=-393.5 kJ·mol-1,ΔH2=-395.4 kJ·mol-1,下列说法或表示中,正确的是( )
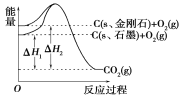
A.金刚石比石墨稳定性好
B.石墨和金刚石的转化是物理变化
C.C(s、石墨)===C(s、金刚石) ΔH=-1.9 kJ·mol-1
D.断裂1 mol石墨中的化学键吸收的能量比断裂1 mol金刚石中的化学键吸收的能量多1.9 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.铜片插入到硝酸银溶液中:Cu+Ag+=Cu2++Ag
B.硫酸镁跟氢氧化钡反应:Ba2++SO42-=BaSO4↓
C.铁片插入盐酸中:2Fe+6H+=2Fe3++3H2↑
D.氢氧化钠溶液和硫酸溶液反应:H++OH-=H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体区别于其它分散系的本质特征是( )
A.胶体粒子直径在1﹣100nm之间
B.胶体粒子带电荷
C.胶体是一种介稳性的分散系
D.光束通过胶体时有丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏德罗常数,下列叙述正确的是( )
A. 标准状况下,22.4L H2O含有的分子数为 NA
B. 常温常压下,1.06g Na2CO3溶于水形成的溶液中含有Na+离子数为0.02 NA
C. 通常状况下,NA个CO2分子占有的体积为22.4L
D. 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有等质量的X、Y两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如右图所示(已知X、Y在生成物中化合价均为+2价)。则下列说法中不正确的是

A. 生成氢气的质量:X﹥Y B. 相对原子质量:X﹥Y
C. 金属活动性:Y﹥X D. 消耗硫酸的质量:X﹥Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,在体积为2L的恒容密闭容器中,某一反应中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列

表述中正确的是
A. 反应的化学方程式为2X = 3Y + Z
B. t时,正、逆反应都不再继续进行,反应达到化学平衡
C. 若t=4,则0~t的X的化学反应速率为0.1 molL-1min-1
D. 温度、体积不变,t时刻充入1 mol He使压强增大,正、逆反应速率都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用软锰矿浆烟气脱硫吸收液制取电解锰,并利用阳极液制备高纯碳酸锰、回收硫酸铵的工艺流程如下(软锰矿的主要成分是MnO2,还含有硅、铁、铝的氧化物和少量重金属化合物等杂质):
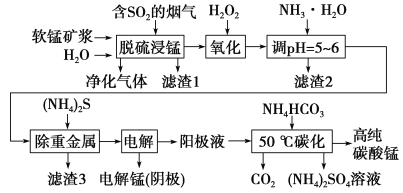
(1)一定温度下,“脱硫浸锰”主要产物为MnSO4,该反应的化学方程式为_______________________。
(2)“滤渣2”中主要成分的化学式为______________。
(3)“除重金属”时使用(NH4)2S而不使用Na2S的原因是______________________。
(4)“电解”时用惰性电极,阳极的电极反应式为_______________________________。
(5)“50 ℃碳化”得到高纯碳酸锰,反应的离子方程式为____________________________。“50 ℃碳化”时加入过量NH4HCO3,可能的原因:使MnSO4充分转化为MnCO3;________________;________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com