
| �� | ����ƽ�ⳣ�� |
| ���� | K i=1.75��10-5 |
| ������ | K i=2.98��10-8 |
| ̼�� | Ki1=4.30��10-7 Ki2=5.61��10-11 |
| ������ | Ki1=1.54��10-2 Ki2=1.02��10-7 |
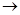 SO32�� + 2HClO
SO32�� + 2HClO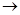 HCO3�� + HClO
HCO3�� + HClO

 ��У��������ĩ��̾�ϵ�д�
��У��������ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ˮ | B�������� | C���ƾ� | D�����ᱵ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������������ˮ�ܵ��磬�ʶ����������ڵ���� |
| B�����ᱵ������ˮ�������ᱵ����������� |
| C��������ǿ����ʣ��ʴ������ܵ��� |
| D��������Ũ����ͬ������ʹ��ᵼ��������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 A-+H+����1.0 mol HA���Ӽ���ˮ���Ƶ�1.0 L��Һ,��ͼ��,��ʾ��Һ��HA��H+��A-�����ʵ���Ũ����ʱ����仯��������ȷ����(����)
A-+H+����1.0 mol HA���Ӽ���ˮ���Ƶ�1.0 L��Һ,��ͼ��,��ʾ��Һ��HA��H+��A-�����ʵ���Ũ����ʱ����仯��������ȷ����(����)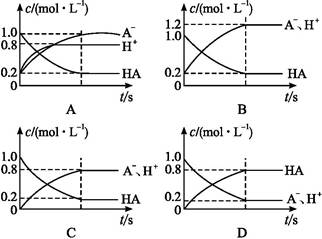
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
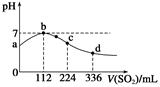
| A��ԭH2S��Һ�����ʵ���Ũ��Ϊ0.05 mol��L��1 |
| B������������Ա������������ǿ |
| C��b��ˮ�ĵ���̶ȱ�c��ˮ�ĵ���̶ȴ� |
| D��a���Ӧ��Һ�ĵ����Ա�d��ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| ʵ���� | HB���ʵ���Ũ��(mol/L) | KOH���ʵ���Ũ��(mol/L) | �����Һ��pH |
| �� | 0.2 | 0.2 | pH��a |
| �� | c1 | 0.2 | pH��7 |
| �� | 0.1 | 0.1 | pH>7 |
| �� | 0.1 | 0.1 | pH��9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������Һϡ�͵�ԭ����� 10�� |
| B�����������Ĵ����ƹ��� |
| C����������0.2 mol��L��1���� |
| D�������Һ���¶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ˮ�����ӻ�����KWֻ���¶��йأ�������ᡢ���һ����Ӱ��ˮ�ĵ���̶� |
| B��Ksp���������ܵ���ʵ����ʺ��¶��йأ�������Һ��������ӵ�Ũ���й� |
| C�������£���0.10 mol��L��1��NH3��H2O��Һ�м�������NH4Cl���壬��ʹ��Һ��pH��С��c��NH4+��/c��NH3��H2O����ֵ���� |
| D�������£�CH3COOH��KW��1.7��10��5��NH3��H2O��Kb��1.7��10��5��CH3COOH��Һ�е�c��H������NH3��H2O�е�c��OH������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com