
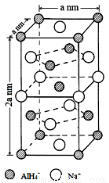
[化学——选修3:物质结构与性质]氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢。NaAlH4可由AlCl3和NaH在适当条件下合成。NaAlH4的晶胞结构如右下图所示。
(1)基态Ti原子的价电子轨道表示式为 。
(2)NaH的熔点为800℃,不溶于有机溶剂。NaH属于 晶体,其电子式为 。
(3)AlCl3在178℃时升华,其蒸气的相对分子质量约为267,蒸气分子的结构式为 (标明配位键)。
(4)AlH4-中,Al的轨道杂化方式为 ;例举与AlH4-空间构型相同的两种离子 (填化学式)。
(5)NaAlH4晶体中,与Na+紧邻且等距的AlH4-有 个;NaAlH4晶体的密度为 g·cm-3(用含a的代数式表示)。若NaAlH4晶胞底心处的Na+被Li+取代,得到的晶体为 (填化学式)。
(6)NaAlH4的释氢机理为:每3个AlH4-中,有2个分别释放出3个H原子和1个Al原子,同时与该Al原子最近邻的Na原子转移到被释放的Al原子留下的空位,形成新的结构。这种结构变化由表面层扩展到整个晶体,从而释放出氢气。该释氢过程可用化学方程式表示为 。
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源:2017届广西省桂林市、崇左市高三联合调研考试理科综合化学试卷(解析版) 题型:选择题
下图是一种酸性燃料电池酒精检测仪,具有自动吹气流量监测与控制的功能,下列有关说法正确的是
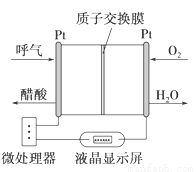
A. 电流由呼气所在的铂电极流出
B. H+透过质子交换膜流向氧气所在的铂电极
C. 电路中流过2mol电子时,消耗11.2LO2
D. 该电池的负极反应为:CH3CH2OH+3H2O-12e-=2CO2↑+12H+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一3月月考化学试卷(解析版) 题型:选择题
化学与环境、生产和生活密切相关,下列说法正确的是( )。
A. 青霉素具有消炎作用,使用前要进行皮肤敏感试验。
B. CO2、NO2或SO2都会导致酸雨的形成。
C. 卫生部公告2011年5月1日起全面叫停面粉增白剂,由此可知:应当严 格禁止在食品中使用任何食品添加剂。
D. 铵态氮肥与熟石灰混合使用可以明显提高肥效。
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三3月月考理科综合化学试卷(解析版) 题型:简答题
a、b、c、d、e是原子序数依次递增的五种短周期元素,其中a元素组成的一种粒子不含电子;b元素的最高价氧化物的水化物甲能与其氢化物生成一种盐乙;d的单质能与酸、碱反应均生成氢气;a,b,d三种元素能与c元素形成常见的化合物;d,e两种元素组成de3型化合物.
(1)写出由以上某些元素构成的既含极性共价键,又含非极性共价键的化合物的电子式_________(写出一种即可)
(2)b的常见氢化物的空间构型是_________:b、c的最简单氢化物中稳定性最强的是_____(填化学式)。
(3)写出三种由以上元素组成的具有漂白性的物质_________(写化学式)。
(4)be3和含有ec2-离子的溶液反应可生成ec2气体和一种碱性气体,写出其离子方程式________.
(5)常温下,甲、乙的水溶液的 pH 均为 5。则两溶液中由水电离出的 H+浓度之比是_________.
(6)由上述元素所形成的常见物质 X、Y、Z、W、M、N 有如下转化关系:

①X 溶液与 Y 溶液反应的离子方程式为___________
②将一小块N的金属箔在酒精灯上加热至熔化后的现象为__________。
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三3月月考理科综合化学试卷(解析版) 题型:选择题
NA为阿伏加罗常数的值,下列说法中正确的是( )
A.44gCO2和N2O的混合物中含有的氧原子数为1.5NA
B.2L0.5mol/L亚硫酸氢钠溶液中含有的HSO3-离子数为NA
C.氢氧化钠与氯气反应时,生成0.1molNaCl转移的电子数为0.1NA
D.一定条件下在密闭容器中2molSO2与2molO2充分反应,最终的气体分子数为3NA
查看答案和解析>>
科目:高中化学 来源:河北省2017届高三下学期三调考试理科综合化学试卷 题型:选择题
分子式为C5H10O2且能与NaOH溶液反应的有机物有(不含立体异构)
A. 13种 B. 4种 C. 9种 D. 16种
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省太原市高一3月阶段性测试化学试卷(解析版) 题型:实验题
某课外活动小组欲利用CuO与氨反应,研究氨的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:
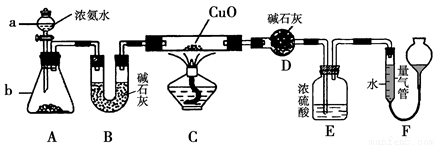
(1)仪器a的名称为____________。
(2)实验室中,利用装置A,还可制取的无色气体是____________(填字母)。
A.Cl2 B.O2
C.CO2 D.NO2
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管内有无色无味的气体生成,上述现象证明氨气具有________性,写出相应的化学方程式___________________。
(4)E装置中浓硫酸的作用_________________。
(5)读取气体体积前,应对装置F进行的操作______________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省太原市高一3月阶段性测试化学试卷(解析版) 题型:选择题
X、Y、Z三种元素位于周期表中同一周期,它们的最高价氧化物分别为酸性氧化物、碱性氧化物、两性氧化物,则三种元素原子序数的大小顺序为( )
A. X>Y>Z B. Y>Z>X C. X>Z>Y D. Z>X>Y
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省桂林市高一下学期开学考试化学试卷(解析版) 题型:填空题
铜是生物体必需的微量元素,也是人类最早使用的金属之一。铜的生产和使用对国计民生各个方面都产生了深远的影响。
(1)为了保护环境和节约资源,通常先用H2O2和稀硫酸的混合溶液溶出废旧印刷电路板中的铜,最终实现铜的回收利用。写出H2O2和稀硫酸的混合溶液与金属铜反应的离子方程式:____________________________________。
(2)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。该工艺的中间过程会发生反应:2Cu2O+Cu2S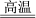 6Cu+SO2↑,该反应的氧化剂是________;当生成19.2 g Cu 时,反应中转移的电子为________ mol。
6Cu+SO2↑,该反应的氧化剂是________;当生成19.2 g Cu 时,反应中转移的电子为________ mol。
(3)研究性学习小组用“间接碘量法”测定某试样中CuSO4·5H2O(不含能与I-反应的氧化性杂质)的含量。称取a g试样配成 100 mL 溶液,取出25.00 mL溶液,向其中滴加 KI 溶液后有白色沉淀生成(发生的反应为2Cu2++4I-===2CuI↓+I2);继续滴加 KI 溶液至沉淀不再产生,反应生成的 I2 与V mL c mol·L-1Na2S2O3溶液恰好完全反应(发生的反应为I2+2Na2S2O3===2NaI+Na2S4O6)。则试样中CuSO4·5H2O的质量分数为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com