
| A£®ĒŠæŖµÄ½šŹōNa±©Ā¶ŌŚæÕĘųÖŠ£¬¹āĮĮ±ķĆęÖš½„±ä°µ2Na+O2=Na2O2 |
| B£®ĻņAgC1Šü×ĒŅŗÖŠµĪ¼ÓNa2SČÜŅŗ£¬°×É«³Įµķ±ä³ÉŗŚÉ«2AgC1+S2- =Ag2S”ż+2C1- |
| C£®Na2O2ŌŚ³±ŹŖµÄæÕĘųÖŠ·ÅÖĆŅ»¶ĪŹ±¼ä£¬±ä³É°×É«Õ³³ķĪļ2Na2O2+CO2=2Na2CO3+O2 |
| D£®ĻņNaHCO3ČÜŅŗÖŠ¼ÓČė¹żĮæµÄ³ĪĒåŹÆ»ŅĖ®£¬³öĻÖ°×É«³Įµķ |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Cl2ĶØČėNaOHČÜŅŗ£ŗCl2£«OH£=Cl££«ClO££«H2O |
| B£®NaHCO3ČÜŅŗÖŠ¼ÓČėĻ”HCl£ŗCO32££«2H£«=CO2”ü£«H2O |
| C£®AlCl3ČÜŅŗÖŠ¼ÓČė¹żĮæĻ”°±Ė®£ŗAl3£«£«4NH3”¤H2O=AlO2££«4NH4£«£«2H2O |
| D£®CuČÜÓŚĻ”HNO3£ŗ3Cu£«8H£«£«2NO3£=3Cu2£«£«2NO”ü£«4H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĻņŅų°±ČÜŅŗÖŠµĪ¼ÓŅŅČ©£ŗ CH3CHO +2[Ag(NH3)2]+ + H2O 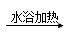 CH3COO£ + NH4+ +3NH3 + 2Ag”ż+2H+ CH3COO£ + NH4+ +3NH3 + 2Ag”ż+2H+ |
B£®±½·ÓÄĘČÜŅŗÖŠĶØČėÉŁĮæCO2£ŗ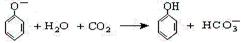 |
| C£®ĮņĖįĒāļ§ČÜŅŗÖŠµĪ¼ÓÉŁĮæNaOHČÜŅŗ£ŗH+£«NH4+£«2OH££½NH3”¤H2O£«H2O |
| D£®ĀČŅŅĖįÓė×ćĮæµÄĒāŃõ»ÆÄĘČÜŅŗ¹²ČČ£ŗCH2ClCOOH£«OH”Ŗ”÷CH2ClCOO”Ŗ£«H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
A£®°±Ė®ÖŠµĪČė·ÓĢŖČÜŅŗ£¬ČÜŅŗ±äŗģ£ŗ NH3”¤H2O  NH4+ + OH”Ŗ NH4+ + OH”Ŗ |
B£®90”ꏱ£¬²āµĆ“æĖ®ÖŠc(H+)”¤c(OH”Ŗ) =3.8”Į10”Ŗ13£ŗ H2O(l)  H+(aq) + OH”Ŗ(aq) H+(aq) + OH”Ŗ(aq)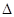 H£¼0 H£¼0 |
C£®FeCl3ČÜŅŗÖŠĶØČėSO2£¬ČÜŅŗ»ĘÉ«ĶŹČ„£ŗ2Fe3++SO2 +2H2O  2Fe2+ + SO42”Ŗ+ 4H+ 2Fe2+ + SO42”Ŗ+ 4H+ |
| D£®Ļņ±½·ÓÄĘČÜŅŗÖŠĶØČėCO2£¬ČÜŅŗ±ä»ė×Ē£ŗ2C6H5ONa£«CO2+H2O ”ś2C6H5OH£«Na2CO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĻņAgClŠü×ĒŅŗÖŠ¼ÓČėNa2SČÜŅŗ£ŗ2AgCl+S2-=Ag2S+2Cl- |
| B£®ĻņNaHCO3ČÜŅŗÖŠ¼ÓČėNaOHČÜŅŗ£ŗHCO3-+OH-= CO32-+H2O |
| C£®ĻņBa£ØOH£©2ČÜŅŗÖŠ¼ÓČėĻ”H2SO4£ŗBa2++OH-+H++ SO42-= BaSO4”ż+ H2O |
| D£®ĻņCu·ŪÖŠ¼ÓČė¹żĮæµÄÅØHNO3£ŗCu+4 H++ 2NO3-= Cu2++2 NO2”ü+2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā

| Ąė×Ó | Ąė×Ó°ė¾¶(pm) | æŖŹ¼³Įµķ Ź±µÄpH | ĶźČ«³Įµķ Ź±µÄpH |
| Fe2£« | 74 | 7.6 | 9.7 |
| Fe3£« | 64 | 2.7 | 3.7 |
| Al3£« | 50 | 3.8 | 4.7 |
| Mn2£« | 80 | 8.3 | 9.8 |
| Pb2£« | 121 | 8.0 | 8.8 |
| Ca2£« | 99 | £ | £ |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
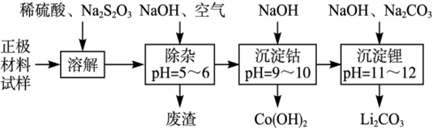
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĻņMg(HCO3)2ČÜŅŗÖŠ¼ÓČė¹żĮæµÄNaOHČÜŅŗ£ŗMg2£«£«2HCO3££«4OH£=Mg(OH)2”ż£«2CO32££«2H2O |
| B£®ĻņNH4Al(SO4)2ČÜŅŗÖŠµĪČėBa(OH)2ČÜŅŗĒ”ŗĆŹ¹SO42£·“Ó¦ĶźČ«£ŗ2Ba2£«£«4OH££«Al3£«£«2SO42£=2BaSO4”ż£«AlO2££«2H2O |
| C£®FeBr2ČÜŅŗÖŠĶØČė¹żĮæµÄCl2£ŗ2Fe2£«£«4Br££«3Cl2=2Fe3£«£«2Br2£«6Cl£ |
| D£®ĻņFe(NO3)2ČÜŅŗÖŠ¼ÓČėĻ”ŃĪĖį£ŗ3Fe2£«£«4H£«£«NO3£=3Fe3£«£«NO”ü£«2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| Ń”Ļī | »Æѧ·“Ó¦ÓėĄė×Ó·½³ĢŹ½ | ĘĄ¼Ū |
| A | ½«ĶŠ¼¼ÓČėŗ¬Fe3£«µÄČÜŅŗÖŠ£ŗ2Fe3£« £«Cu=2Fe2£«£«Cu2£« | ÕżČ· |
| B | Na2O2ÓėH2O·“Ó¦£ŗNa2O2£« H2O=2Na£«£«2OH££«O2”ü | “ķĪó£¬ŃõŌŖĖŲ²»ŹŲŗć |
| C | NaOHČÜŅŗÓėŃõ»ÆĀĮ·“Ó¦£ŗAl2O3£« 2OH£=2AlO2-£«H2O | “ķĪ󣬲śĪļÓ¦øĆŹĒAl(OH)3 |
| D | ĻņFe(OH)2ÖŠ¼ÓČė×ćĮæĻ”ĻõĖį£ŗ Fe(OH)2£«2H£«=Fe2£«£«2H2O | “ķĪó£¬HNO3ÄÜŃõ»ÆFe2£« |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com