
在0.1 mol/l的NH3·H2O溶液中,下列关系正确的是
A.C(NH3·H2O)>C(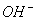 )>C(
)>C(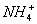 )>C(H+)
)>C(H+)
B.C(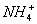 )>C(NH3·H2O)>C(
)>C(NH3·H2O)>C(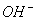 )>C(H+)
)>C(H+)
C.C(NH3·H2O)>C(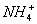 )=C(
)=C(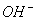 )>C(H+)
)>C(H+)
D.C(NH3·H2O)>C(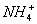 )>C(H+)>C(
)>C(H+)>C(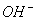 )
)
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
某同学为了测定三聚氰胺的分子式,设计了如下实验:
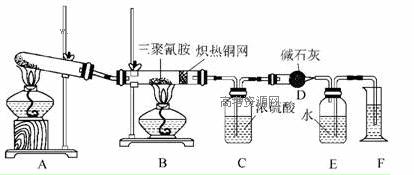
查阅资料,三聚氰胺的相对分子质量为126,在常温下为晶体,由碳、氢、氮三种元素组成,加热条件下能与氧气发生反应生成二氧化碳、氮气和水。取12.6 g三聚氰胺晶体按图示实验装置进行三聚氰胺与氧气的反应(假设三聚氰胺完全转化成产物),并通过测定生成物的量计算三聚氰胺的分子组成。
(1)写出A装置中发生反应的化学方程式_______________________________________。
(2)C装置能不能与D装置互换?__________(填“能”或“不能”)。理由是__________________________。
(3)当B装置中反应完全发生后,读取F中水的体积的实验操作顺序为__________(填序号)。
①读数 ②冷却至室温 ③调平E、F装置中的液面
(4)测定数据如下:
| 装置 | C | D |
| 实验前 | 101.0 g | 56.0 g |
| 实验后 | 106.4 g | 69.2 g |
经测定,E中收集的气体折合成标准状况下的体积为6.72 L。
①利用上述实验数据,计算三聚氰胺的分子式为__________。
②若B装置中没有铜网,对测定结果的影响是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式与所述事实相符且正确的是
A.漂白粉溶液在空气中失效: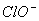 +CO2+H2O=HClO+
+CO2+H2O=HClO+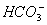
B.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl- Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
C.向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O=Al(OH)3↓+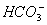
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3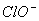 +2Fe(OH)3=2
+2Fe(OH)3=2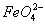 +3
+3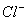 +H2O+4H+
+H2O+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
水体中重金属铅的污染问题备受关注。水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)3-、Pb(OH)42-,各形态的浓度分数α随溶液pH变化的关系如图所示:
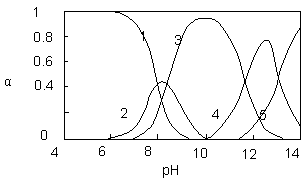
【1表示Pb2+,2表示Pb(OH)+,3表示Pb(OH)2,4表示Pb(OH)3-,5表示Pb(OH)42-】
⑴Pb(NO3)2溶液中,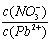 2 (填“>”、“=”、“<”);往该溶液中滴入氯化铵溶液后,
2 (填“>”、“=”、“<”);往该溶液中滴入氯化铵溶液后,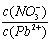 增加,可能的原因是 。
增加,可能的原因是 。
⑵往Pb(NO3)2溶液中滴稀NaOH溶液,pH=8时溶液中存在的阳离子(Na+除外)有
,pH=9时,主要反应的离子方程式为 。
⑶某课题组制备了一种新型脱铅剂,能有效去除水中的痕量铅,实验结果如下表:
 |
 离子 Pb2+ Ca2+ Fe3+ Mn2+ Cl-
离子 Pb2+ Ca2+ Fe3+ Mn2+ Cl-
处理前浓度/(mg·L-1) 0.20130 29.8 0.120 0.087 51.9
处理后浓度/(mg·L-1) 0.004 22.6 0.040 0.053 49.8
 上表中除Pb2+外,该脱铅剂对其它离子的去除效果最好的是 。
上表中除Pb2+外,该脱铅剂对其它离子的去除效果最好的是 。
⑷如果该脱铅剂(用EH表示)脱铅过程中主要发生的反应为:
2EH(s)+Pb2+ E2Pb(s)+2H+
E2Pb(s)+2H+
则脱铅的最合适pH范围为 (填代号)。
A.4~5 B.6~7 C.9~2013 D.2013~12
查看答案和解析>>
科目:高中化学 来源: 题型:
25ºC,若12体积的某强碱溶液与1体积的某强酸溶液混合后,溶液呈中性,则混合之前,
该碱的pH与强酸的pH之间该满足的关系是_______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
向体积为0.05mol·L-1CH3COOH溶液中加入体积为Vb的0.05mol·L-1KOH溶液,下列关系错误的是
A. Va>Vb时:c (CH3COOH) +c (CH3COO-)>c (K+)
B. Va=Vb时:c (CH3COOH) +c (H+)>c (OH-)
C. Va<Vb时:c (CH3COO-)>c (K+)> c (OH-)> c (H)
D. Va与Vb任意比时:c (K+)+ c (H+) =c (OH-)+ c (CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
浓度都是1 mol·L-1的四种正盐溶液:AX、BX、AY、BY;AX的溶液pH=7且溶液中 c(x-)=1 mol·L-1,BX的溶液pH=4,BY的溶液pH=6。则AY的溶液pH为 ( )
A.大于7 B.等于7 C.小于7 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
反应2H2S(g)  2H2(g)+S2(g) ΔH >0,其他条件不变,下列说法正确的是
2H2(g)+S2(g) ΔH >0,其他条件不变,下列说法正确的是
A.加入催化剂,反应路径将发生改变,ΔH也将随之改变
B.升高温度,正逆反应速率都增大,H2S分解率也增大
C.增大压强,平衡向逆反应方向移动,体系温度降低
D.恒容体系,充入H2重新达到平衡后,H2浓度将减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com