
【题目】(题文)有X、Y、Z三种短周期元素,原子半径大小关系为r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质分子在适当条件下可发生如图变化,其中B和C均为10电子分子.下列说法中不正确的是
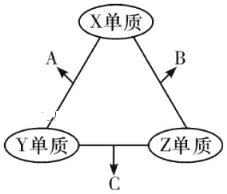
A. X与Z形成的某种化合物可用来杀菌消毒 B. C极易溶于B中,溶液呈碱性
C. Y与Z形成的二元化合物只含有极性键 D. A和C能发生氧化还原反应
科目:高中化学 来源: 题型:
【题目】在实验中,用镊子从煤油中取出一小块金属钠,然后用滤纸将煤油吸干,再用小刀切开观察。在这一实验过程中不能得出的钠的物理性质是
A. 钠在常温下是固体 B. 钠的熔点很低
C. 钠具有银白色的金属光泽 D. 金属钠很软
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1~18号元素的离子![]() 都具有相同的电子层结构,则下列叙述或表示方法正确的是
都具有相同的电子层结构,则下列叙述或表示方法正确的是
A. 四种元素位于同一周期
B. 氢化物的稳定性H2Y>HZ
C. 离子的氧化性![]()
D. a+3<c-2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有室温下四种溶液,有关叙述不正确的是( )
① | ② | ③ | ④ | |
pH | 11 | 11 | 3 | 3 |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
A. ①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
B. 分别加水稀释10倍,四种溶液的pH ①>②>④>③
C. ①、④两溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D. VaL④与VbL②溶液混合后,若混合后溶液pH=4,则Va∶Vb=11∶9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛铁矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有少量MgO、CaO、SiO2等杂质。利用钛铁矿制备锂离子电池电极材料(钛酸锂Li4Ti5O12和磷酸亚铁锂LiFePO4)的工艺流程如下图所示:

(1)化合物Li2Ti5O15中钛元素的化合价是+4价,氧元素的化合价为__________。
(2)钛铁矿与硫酸反应时,常将钛铁矿粉碎,其目的是:__________,滤渣A的成分是__________。
(3)固体TiO2转化(NH4)2Ti5O15的离子方程式为__________,该反应__________氧化还原反应 (填“属于” 或“不属于” )。
(4)反应②中固体TiO2、转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如图所示。反应温度过高时,Ti 元素浸出率下降的原因是__________。

(5)(NH4)2Ti5O15转化为Li2Ti5O15的离子方程式为:__________。
(6)写出由滤液D生成FePO4的离子方程式__________。
(7)由滤液D制各LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是批量生产的笔记本电脑所用的甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应。电池总反应式为2CH3OH+3O2===2CO2+4H2O。下列说法中不正确的是
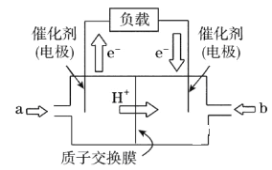
A. 左边的电极为电池的负极,a处通入的是甲醇
B. 每消耗3.2 g氧气转移的电子为0.4 mol
C. 电池负极的反应式为CH3OH+H2O6e===CO2+6H+
D. 电池的正极反应式为O2+2H2O+4e===4OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,说明金刚石和石墨是同素异形体的是
A.它们都是熔、沸点很高的晶体
B.它们都是不溶于水的单质
C.二者是不同的单质,在一定条件下能相互转化
D.二者的结构不同,但化学性质相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取氯气有下列反应:2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O
(1)该反应中氧化剂是_____;被还原的元素是_______;氧化产物是 ______;
(2)用单线桥法标出电子转移的方向和数目______________;
(3)若该反应中有0.2mol的电子转移,则能生成标准状况下的氯气的体积是_______;
(4)若该反应有1molKMnO4参加反应,被氧化的HCl为______mol,转移电子数______mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com