
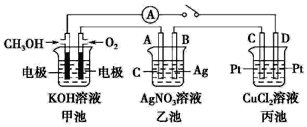
【题目】某化学兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装 置的开关时,观察到电流表的指针发生了偏转。
请回答下列问题:
(1)甲池为原电池,通入 CH3OH 电极的电极反应为________。
(2)乙池中A(石墨)电极的名称为_____(填“正极”“负极”或“阴极”“阳极”),总反应为_____。
(3)当乙池B极质量增加 5.4 g 时,甲池中理论上消耗 O2 的体积为_____mL(标准状况),丙池D极析出_____g 铜。
【答案】CH3OH+8OH--6e-=CO32-+6H2O 阳极 4AgNO3+2H2O![]() 4Ag+O2↑+4HNO3 280 1.6
4Ag+O2↑+4HNO3 280 1.6
【解析】
(1)甲池为原电池,通入 CH3OH 电极为负极,负极上CH3OH失去电子,发生氧化反应,在碱性溶液中被氧化生成CO32-,则该电极的电极反应为CH3OH+8OH--6e-=CO32-+6H2O;
(2)乙池中A(石墨)电极与电源的正极相连,作阳极,溶液中的OH-失去电子,发生氧化反应,电极反应式为:4OH- -4e-=2H2O+O2↑,阴极B(Ag)电极上,溶液中的Ag+获得电子,发生还原反应,电极反应式为Ag++e-=Ag,在同一闭合回路中电子转移数目相等,可得总反应方程式为:4AgNO3+2H2O![]() 4Ag+O2↑+4HNO3;
4Ag+O2↑+4HNO3;
(3)当乙池B极质量增加 5.4 g 时,n(Ag)=5.4g÷108g/mol=0.05mol,则电路中通过电子物质的量为0.05mol,由于在串联电路中电子转移数目相同,所以甲池中理论上消耗 O2 的物质的量为n(O2)=0.05mol÷4=0.0125mol,则氧气在标准状况下体积为V(O2)=0.0125mol×22.4L/mol=0.28L=280mL,丙池与甲、乙池串联,电子转移的物质的量也是0.05mol,D极电极反应式为Cu2++2e-=Cu,所以D极析出Cu的物质的量为0.05mol÷2=0.025mol,m(Cu)=0.025mol×64g/mol=1.6g 。


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是( )
A. NH3·H2O的电离平衡常数随着温度升高而减小
B. 在0.10 mol·L-1 CH3COOH溶液中,加入少量CH3COONa晶体后,溶液的pH减小
C. 强酸、强碱和大部分盐类都是强电解质,其他化合物都是弱电解质
D. 相同温度下,醋酸溶液的导电能力可能比稀硫酸强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】400 ℃时,某密闭容器中有X、Y、Z三种气体,从反应开始到达到平衡时各物质浓度的变化如图甲所示(假定反应向正反应方向进行)。图乙为相应时刻仅改变反应体系中某一条件后正、逆反应速率随时间变化的情况。
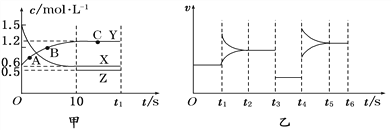
(1)反应从开始至平衡时v(X)=________________;A、B、C三点的逆反应速率由大到小的顺序为_______________________________________________。
(2)若t3 s时改变的条件是降低压强,则Z物质的起始浓度是________;400 ℃时该反应的平衡常数为________。
(3)t4 s时改变的条件是________,若该反应具有自发性,则此时平衡向________________(填“正反应方向”或“逆反应方向”)移动。
(4)在图乙中绘制出t6 s时向容器中加入一定量X后建立新平衡的过程中(压强保持不变)正、逆反应速率的变化曲线并注明速率类型。____________________
(5)研究表明,该反应经过如下几个阶段:
3X(g)![]() 2Q(s)+P(g) ΔH1 Q(s)===Y(g)+W(g) ΔH2 P(g)+2W(g)
2Q(s)+P(g) ΔH1 Q(s)===Y(g)+W(g) ΔH2 P(g)+2W(g)![]() Z(g) ΔH3
Z(g) ΔH3
试写出X、Y、Z间反应的热化学方程式________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于Na和Na+的叙述中,错误的是
A. 它们相差一个电子层
B. 它们的化学性质相似
C. 钠原子,钠离子均为同一元素
D. 灼烧时,它们的焰色反应都呈黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
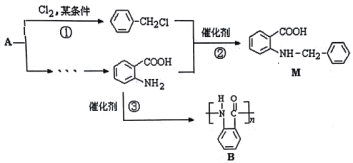
【题目】化合物M是一种合成药品的中间体,其合成路线如图所示。
已知: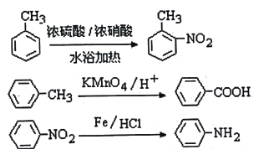
(弱碱性,易被氧化)
(1)写出反应①的化学方程式_____________。
(2)反应②属于____反应(填有机反应类型)。
(3)写出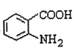 中官能团的名称__________。
中官能团的名称__________。
(4)H为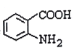 的同分异构体,则满足下列条件的H的同分异构体共有______种,其中满足下列条件且含4种不同氢原子的同分异构体的结构简式是___________。
的同分异构体,则满足下列条件的H的同分异构体共有______种,其中满足下列条件且含4种不同氢原子的同分异构体的结构简式是___________。
①显弱碱性,易被氧化 ②分子内含有苯环 ③能发生水解反应
(5)请你设计由A合成B的合成路线_________________________________________________________。
提示:①合成过程中无机试剂任选; ②合成路线表示方法示例如图所示。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)(题文)在恒温、恒容条件下,能说明可逆反应:H2(g)+I2(g) 2HI(g)达到平衡状态的是
A. 气体的压强保持不变 B. v(H2)正=2v(HI)逆
C. 气体的密度保持不变 D. 气体的颜色保持不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com