
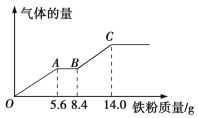
【题目】现有某稀硫酸和稀硝酸的混合溶液200 mL,将其平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g铜粉;向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化关系如图所示(假设硝酸的还原产物为NO气体)。下列分析或结果正确的是
A. 原混合溶液中NO3-的物质的量为0.2 mol
B. OA段产生的是氢气
C. BC段产生NO
D. 原混合溶液中H2SO4的浓度为1.25mol/L
【答案】A
【解析】
铁粉既能和稀硝酸反应也能和稀硫酸反应,硝酸的氧化性比硫酸强,所以硝酸先发生反应。由图象可知在铁过量时, OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段发生反应为:Fe+2Fe3+=3Fe2+,BC段发生反应为:Fe+2H+=Fe2++H2↑。据此解答。
A.OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,硝酸全部起氧化剂作用,每一份溶液中n(NO3-)=n(Fe),所以原混合酸中n(HNO3)=2n(Fe)=2×![]() ,A正确;
,A正确;
B.OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,可见OA产生的气体是NO,不是氢气,B错误;
C.在BC段发生反应为:Fe+2H+=Fe2++H2↑,可见BC段产生的气体是H2,C错误;
D.根据图像可知:当加入Fe粉14g时,气体飞物质的量不再增加,此时溶液中溶质为FeSO4,此时反应消耗铁的物质的量n(Fe)=![]() =0.25mol,根据元素原子守恒可知n(H2SO4)=n(FeSO4)=n(Fe)=0.25mol,故硫酸的浓度是c(H2SO4)=
=0.25mol,根据元素原子守恒可知n(H2SO4)=n(FeSO4)=n(Fe)=0.25mol,故硫酸的浓度是c(H2SO4)=![]() =2.5mol/L,由于溶液有均一性,溶液的浓度与体积无关,所以原混合溶液中H2SO4的浓度为2.5mol/L,D错误;
=2.5mol/L,由于溶液有均一性,溶液的浓度与体积无关,所以原混合溶液中H2SO4的浓度为2.5mol/L,D错误;
故合理选项是D。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列关于浓HNO3和浓H2SO4的叙述中不正确的是( )
A. 常温下二者都可用铁制容器贮存
B. 常温下二者都能与铜较快反应
C. 露置于空气中,溶液浓度均降低
D. 浓HNO3与浓H2SO4都具有强氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业的味精”。钒对稀酸是稳定的,但室温下能溶解于浓硝酸中生成![]() 。
。
(1)请写出金属钒与浓硝酸反应的离子方程式:________________________
(2)灼烧![]() 时可生成钒的氧化物
时可生成钒的氧化物![]() 请写出该反应的化学方程式:_________
请写出该反应的化学方程式:_________
(3)![]() 是较强的氧化剂。它能与沸腾的浓盐酸作用产生氯气,其中钒元素被还原为蓝色的
是较强的氧化剂。它能与沸腾的浓盐酸作用产生氯气,其中钒元素被还原为蓝色的![]() 请写出该反应的离子方程式:________________________
请写出该反应的离子方程式:________________________
(4)![]() 是两性氧化物,与强碱反应生成钒酸盐(阴离子为
是两性氧化物,与强碱反应生成钒酸盐(阴离子为![]() ),溶于强酸生成含钒氧离子
),溶于强酸生成含钒氧离子![]() 的盐。请写出
的盐。请写出![]() 分别与烧碱溶液和稀硫酸反应生成的盐的化学式:
分别与烧碱溶液和稀硫酸反应生成的盐的化学式:
______________________
(5)工业上用接触法制硫酸时要用到![]() 。在氧化
。在氧化![]() 的过程中,450℃时发生
的过程中,450℃时发生![]() 与
与![]() 之间的转化:
之间的转化:![]() 说明
说明![]() 在接触法制硫酸过程中所起的作用是________________________
在接触法制硫酸过程中所起的作用是________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,0.1mol/L的Na2CO3溶液中,下列粒子浓度关系式不正确的是
A. c(Na+)= 2[c(CO32-)+ c(HCO3-)+ c(H2CO3)]
B. c(Na+)+ c(H+)= 2c(CO32-)+ c(HCO3-)+ c(OH—)
C. c(H+)= c(OH-)—c(HCO3-)—c(H2CO3)
D. c(Na+)>c(CO32-)> c(OH—)> c(HCO3-)> c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于元素周期表和元素周期律的应用有如下叙述:其中正确的是( )
①元素周期表是同学们学习化学知识的一种重要工具;
②利用元素周期表可以预测新元素的原子结构和性质;
③利用元素周期表和元素周期律可以预言新元素;
④利用元素周期表可以指导寻找某些特殊的材料。
A. ①②③④ B. ②③④ C. ③④ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇(CH3OH)是重要的溶剂和替代燃料,工业上用CO和H2在一定条件下制备CH3OH的反应为: CO(g)+2H2(g)![]() CH3OH(g) ΔH
CH3OH(g) ΔH
(1)T℃时,在体积为1L的恒容密闭容器中,充入2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图一所示。
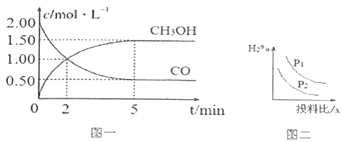
①反应2min到5min,用氢气表示的平均反应速率v(H2)=___________。
②下列说法正确的是______________(填字母序号)。
A.达到平衡时,CO的转化率为50%
B.5min后容器中压强不再改变
C.达到平衡后,再充入氩气,反应速率增大
D.2min前v(正)>v(逆),2min后v(正)<v(逆)
E.加入催化剂可以加快化学反应速率,同时提高 CO和H2平衡的转化率
③下列叙述可以说明该反应在该条件下已经达到化学平衡的是:______(填字母序号)。
A.混合气体密度不发生改变 B.混合气体的平均相对分子质量不再发生改变
C.v(CO)正=2v(H2)逆D.n(CO)与n(H2)的比值不变
(2)某温度下,在一容积可变的恒压密闭容器中分别充入1molCO和1.2molH2,达到平衡时容器体积为2L,且含有0.5molCH3OH(g),则该反应平衡常数的值为_______,此时向容器中再通入0.3molCO和0.3molCH3OH(g),则此平衡将______________移动。(填“向正反应方向”、“不”或“向逆反应方向”)
(3)若压强、投料比x=n(CO)/n(H2)对反应的影响如图二所示,则图中曲线所示的压强关系:p1_____p2(填“=”“>”或“<”)。
(4)工业上另一种合成甲醇的方法是利用CO2和H2,己知:CH3OH、H2的燃烧热(ΔH)分别为-726.9kJ/mol、-285.8kJ/mol,则常温下CO2和H2反应生成CH3OH(l)和H2O(l)的热化学方程式______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(13分)用辉铜矿(主要成分为 Cu2S,含少量Fe2O3、SiO2,等杂质)制备难溶于水的碱式碳酸铜的流程如下:

(1)下列措施是为了加快浸取速率,其中无法达到目的的是____(填字母)。
A.延长浸取时间 | B.将辉铜矿粉碎 |
C.充分搅拌 | D.适当增加硫酸浓度 |
(2)滤渣I巾的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的离子方程式:_______。
(3)研究发现,若先除铁再浸取,浸取速率明显变慢,可能的原因是___________。
(4)“除铁”的方法是通过调节溶液pH,使Fe3+转化为Fe(OH)3,则加入的试剂A可以是_______(填化学式);“赶氨”时,最适宜的操作方法是________。
(5)“沉锰”(除Mn2+)过程中有关反应的离子方程式为_______。
(6)滤液Ⅱ经蒸发结晶得到的盐主要是___________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化不属于水解反应的是
A.吃馒头时多咀嚼后有甜味
B.不慎将浓硝酸沾到皮肤上会出现黄色斑痕
C.油脂和氢氧化钠溶液共热后可制得肥皂
D.蛋白质在胃蛋白酶或胰蛋白酶作用下转变为氨基酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识,回答下列问题:
Ⅰ.在① ![]() ②
② ![]() ③
③ ![]() ④
④ ![]() ⑤
⑤![]() ⑥
⑥ ![]() 中:
中:
(1)____和____互为同位素。
(2)____和____质量数相等,但不能互称同位素。
(3)____和____的中子数相等,但质子数不相等,所以不是同一种元素。
Ⅱ.已知31 g白磷变为31 g红磷释放能量。试回答:
(1)上列变化属于_____________变化。
(2)31 g白磷具有的能量_________(填“>”或“<”,下同)31 g红磷具有的能量。
(3)31 g白磷完全燃烧释放的能量_________31 g红磷完全燃烧释放的能量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com