
| A. | NH3 H2O | B. | CO2 HCl | C. | NO H2 | D. | CH4 Br2 |
分析 由同种原子构成的共价键是非极性键,不同原子构成的共价键是极性键,分子中正负电荷中心不重合,从整个分子来看,电荷的分布是不均匀的,不对称的,这样的分子为极性分子,以极性键结合的双原子一定为极性分子,以极性键结合的多原子分子如结构对称,正负电荷的重心重合,电荷分布均匀,则为非极性分子.
解答 解:A、NH3 和 H2O都是极性分子,故A正确;
B、二氧化碳是非极性分子,氯化氢是极性分子,故B错误;
C、一氧化氮是极性分子,而氢气是非极性分子,故C错误;
D、甲烷和溴单质都是非极性分子,故D错误;
故选A.
点评 本题考查化学键与分子的极性的关系,难度不大,注意非极性分子的结构对称,正负电荷中心重合来解答,侧重于考查学生对基础知识的应用能力.


 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:实验题
| 实验步骤 | 实验结论 氧化性从强到弱的顺序:氯、溴、碘 |
| ①氯水+1mL CCl4,振荡,静置,观察四氯化碳层颜色 | |
| ②NaBr溶液+氯水+1mL CCl4,振荡,静置,观察四氯化碳层颜色 | |
| ③KI溶液+氯水+1mL CCl4,振荡,静置,观察四氯化碳层颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
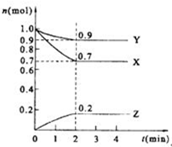 某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在同温同压时,相同体积的任何气体单质所含的原子数目相同 | |
| B. | 2 g 氢气所含原子数目为 NA | |
| C. | 在常温常压下,11.2 L 氮气所含的原子数目为 NA | |
| D. | 17 g 氨气所含电子数目为 10 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位时间生成 n mol 的 A2,同时生成 n mol 的 AB | |
| B. | 容器内的总压强不随时间的变化而变化 | |
| C. | 单位时间生成2n mol 的 AB,同时生成n mol 的 B2 | |
| D. | 单位时间生成n mol 的 A2,同时生成n mol 的 B2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
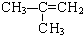 互为同分异构体,关于它们的性质叙述正确的是( )
互为同分异构体,关于它们的性质叙述正确的是( )| A. | 它们的分子式相同,物理性质相同 | |
| B. | 它们都具有碳碳双键,与H2加成的产物完全相同 | |
| C. | 它们都能使酸性高锰酸钾溶液褪色 | |
| D. | 它们都符合通式CnH2n-2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
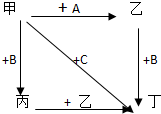 图中,乙是一种非金属单质,通常为黄绿色气体,A为一种黑色粉状固体,B是一种常见的金属单质,C是一种红褐色物质,它们之间存在如图关系:
图中,乙是一种非金属单质,通常为黄绿色气体,A为一种黑色粉状固体,B是一种常见的金属单质,C是一种红褐色物质,它们之间存在如图关系:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
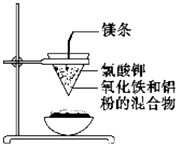 如图所示:用两张圆形滤纸分别折叠成漏斗状,套在一起,使四周都有四层.把内层滤纸取出,在底部剪一个小孔,用水润湿,再跟另一纸漏斗套在一起,架在铁圈上,下面放置一盛沙的蒸发皿.把5g干燥的氧化铁粉末和2g铝粉混合均匀,放在纸漏斗中,上面加少量氯酸钾并在混合物中间插一根镁条,用小木条点燃镁条.观察发生的现象.通过以上实验信息,回答下列问题:
如图所示:用两张圆形滤纸分别折叠成漏斗状,套在一起,使四周都有四层.把内层滤纸取出,在底部剪一个小孔,用水润湿,再跟另一纸漏斗套在一起,架在铁圈上,下面放置一盛沙的蒸发皿.把5g干燥的氧化铁粉末和2g铝粉混合均匀,放在纸漏斗中,上面加少量氯酸钾并在混合物中间插一根镁条,用小木条点燃镁条.观察发生的现象.通过以上实验信息,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com