
【题目】乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4·xH2O)进行的探究性学习的过程。 请你参与并协助他们完成相关学习任务。该组同学的研究课题是:探究测定草酸晶体(H2C2O4xH2O)中的x值。通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定.学习小组的同学设计了滴定的方法测定x值.
①称取2.520g纯草酸晶体,将其制成100.00mL水溶液为待测液。
②取25.00mL待测液放入锥形瓶中,再加入适量的稀H2SO4.
③用浓度为0.1000molL-1 的KMnO4标准溶液进行滴定,达到终点时消耗20.00mL。
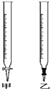
(1)滴定时,将酸性KMnO4标准液装在如图中的______(填“甲”或“乙”)滴定管中。
(2)本实验滴定达到终点的标志是________________;
(3)通过上述数据,求得x=______;
讨论:①若滴定终点时仰视滴定管刻度,则由此测得的x值会______(填“偏大”、“偏小”或“不变”,下同);
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的x会__________。
【答案】 甲 当滴最后一滴KMnO4溶液时,溶液由无色变为紫色,且半分钟内不褪色 2 偏小 偏小
【解析】(1)因为KMnO4具有强氧化性,会腐蚀橡胶管,故应用酸式滴定管盛装,故答案为:甲;(2)可利用KMnO4溶液自身的颜色作为指示剂判断滴定终点时,再滴加KMnO4溶液时,溶液将由无色变为紫色,故答案为:当滴入最后一滴KMnO4溶液时,溶液由无色变为紫色,且半分钟内不褪色,即达滴定终点;(3)由题给化学方程式及数据可知,2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O;2.520g纯草酸晶体中含H2C2O4的物质的量为:0.100 0 mol/L×20.00 mL×10-3 L/mL×![]() =0.0200 mol,0.02molH2C2O4的质量为0.02mol×90g/mol=1.8g,所以2.520g H2C2O4xH2O中水的物质的量为2.520g-1.8g=0.72g,其物质的量=
=0.0200 mol,0.02molH2C2O4的质量为0.02mol×90g/mol=1.8g,所以2.520g H2C2O4xH2O中水的物质的量为2.520g-1.8g=0.72g,其物质的量=![]() =0.04mol,则x=2,故答案为:2;(3)①若滴定终点时仰视滴定管读数,则所得消耗酸性KMnO4溶液的体积偏大,由此所得n(H2C2O4)偏大,则n(H2O)偏小,x偏小;故答案为:偏小;②同理,若酸性KMnO4溶液因久置而导致浓度变小,则消耗其体积偏大,所得x值偏小,故答案为:偏小。
=0.04mol,则x=2,故答案为:2;(3)①若滴定终点时仰视滴定管读数,则所得消耗酸性KMnO4溶液的体积偏大,由此所得n(H2C2O4)偏大,则n(H2O)偏小,x偏小;故答案为:偏小;②同理,若酸性KMnO4溶液因久置而导致浓度变小,则消耗其体积偏大,所得x值偏小,故答案为:偏小。


科目:高中化学 来源: 题型:
【题目】在一定温度时,N2与H2反应过程中能量变化的曲线如图,下列叙述正确的是

A. 该反应的热化学方程式为:N2+3H2![]() 2NH3 △H=-92kJ/mol
2NH3 △H=-92kJ/mol
B. a曲线是加入催化剂时的能量变化曲线
C. 加入催化剂,该化学反应的放热减少
D. 反应物的总能量高于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取50.0 mL Na2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到14.51 g白色沉淀,用过量稀硝酸处理后沉淀量减少到4.66 g,并有气体放出。试计算:
(1)写出Na2SO4的电离方程式;
(2)原混合溶液中Na2CO3和Na2SO4的物质的量浓度;
(3)产生的气体在标准状况下的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,向100 mL H2S饱和溶液中通入SO2气体,所得溶液pH变化如图所示。下列分析正确的是

A. a点对应溶液的导电性比d点强
B. 氢硫酸的酸性比亚硫酸的酸性强
C. 向d点对应的溶液中加入Ba(NO3)2溶液,产生BaSO4白色沉淀
D. H2S饱和溶液的物质的量浓度为0.05 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据图中A~I均为中学化学中常见物质.其中A、B、 C、D为单质,通常情况下A为黄绿色气体,B为固体,C、D为无色气体:其余为化合物,其中常温下E是无色气体.其水溶液为强酸,G是具有磁性的物质,常温下I为液体。
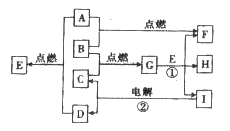
(1)写出下列物质的化学式:A________;F______;G_________。
(2)反应①的离子方程式为______________________________________。
(3)实验室要除去A气体中少量E,将混和气体通过盛有__________的洗气瓶洗气。
(4)F、 H可相互转化,写出一种F转化为H的化学方程式:__________________。
(5)请设计一组实验方案检验F中阳离子:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知A是常用来衡量一个国家石油化工发展水平的标志性物质,A、B、C、D、F、G均为有机物,它们之间有如图转化关系,请回答下列问题:

(1)写出A中官能团的名称:A________,B中官能团的电子式B_______________。
(2)写出与F互为同系物的含5个碳原子的所有同分异构体中一氯代物种类最少的物质的结构简式:______。
(3)写出下列编号对应反应的化学方程式,并注明反应类型:
②____________________, _________________反应;
④________________________ , ________________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. HCl溶液中无OH- B. NaOH溶液中无H+
C. KCl溶液中既无H+也无OH- D. 常温下,任何物质的水溶液中都有H+和OH-,且KW=1×10-14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1774年瑞典化学家舍勒用软锰矿(主要成分是二氧化锰)和浓盐酸共热得到黄绿色气体。甲、乙两个同学分别采取上述反应原理,各制取一瓶氯气,用其验证Cl2与水反应产物的性质。甲、乙同学采用的装置如下图所示:


回答下列问题:
(1)写出实验中制备氯气的化学方程式________________。
(2)对于乙同学的实验装置,要停止实验,其操作顺序是____________。
①停止加热 ②取出集气瓶盖好 ③将导管伸入到烧碱溶液中
(3)甲、乙两同学分别往收集到的氯气中加入适量的水,充分振荡后将所得溶液与NaHCO3粉末反应,有无色气体产生,从而得Cl2与水反应的产物具有较强的酸性的结论。
你认为甲、乙两同学所得结论合理吗?甲:_________,乙:__________。
不合理的说明理由:________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com