
【题目】下表是一些烷烃的燃烧热,则下列表达正确的是
化合物 | 燃烧热/ kJ·mol-1 | 化合物 | 燃烧热/ kJ·mol-1 |
甲烷 | 891.0 | 正丁烷 | 2878.0 |
乙烷 | 1560.8 | 异丁烷 | 2869.6 |
丙烷 | 2221.5 | 异戊烷 | 3531.3 |
A. 正戊烷的燃烧热大于3531.3 kJ·mol-1
B. 相同质量的烷烃、碳的质量分数越大,燃烧放出的热量越多
C. 正丁烷转化为异丁烷的热化学方程式为:CH3CH2CH2CH3(g) ![]() CH3CH(CH3)CH3(g) △H =+8.4kJ·mol-1
CH3CH(CH3)CH3(g) △H =+8.4kJ·mol-1
D. 甲烷燃烧的热化学方程式为:CH4(g)+2O2(g) ![]() CO2(g) +2H2O(g) △H =-891.0kJ·mol-1
CO2(g) +2H2O(g) △H =-891.0kJ·mol-1
【答案】A
【解析】
A、正戊烷和异丁烷互为同分异构体,由表格正丁烷、异丁烷的燃烧热比较可知,则互为同分异构体的化合物,支链多的燃烧热小,则正戊烷的燃烧热大于异戊烷,即正戊烷的燃烧热大于3531.3KJ/mol,故A正确;B.相同质量的烷烃,氢的质量分数越大,燃烧放热越多,故B错误;C.由表格的数据可知,异丁烷的燃烧热比正丁烷的燃烧热小,则异丁烷的能量低,正丁烷转化为异丁烷为放热反应,△H<0,故C错误;D、根据燃烧热的含义:完全燃烧1mol甲烷生成二氧化碳和液态水时会放出891.0KJ的热量,所以热化学方程式为CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-891.0kJ/mol,故D错误;故选A。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列方程式书写不正确的是( )
A. 乙烯使溴的四氯化碳溶液褪色: Br2+ CH2=CH2→ CH2BrCH2Br
B. 用惰性电极电解氯化钠溶液: 2Cl -+ 2H2O![]() H2+Cl2↑+ 2OH-
H2+Cl2↑+ 2OH-
C. 实验室制乙炔: CaC2 + 2H2O → C2H2↑ + Ca(OH)2
D. 溴乙酸与氢氧化钠溶液共热: BrCH2COOH+OH-![]() BrCH2COO-+H2O
BrCH2COO-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在①、②、③容积不等的恒容密闭容器中,均充入0.1molCO和0.2molH2,在催化剂的作用下发生反应:CO(g)+2H2(g)![]() CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示:下列说法正确的是( )
CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示:下列说法正确的是( )
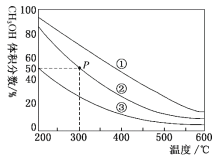
A.该反应的正反应为吸热反应
B.三个容器容积:①>②>③
C.在P点,CO转化率为75%
D.在P点,向容器②中再充入CO、H2及CH3OH各0.025mol,此时v(CO)正>v(CO)逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组利用如图装置制备 NH3 并探究其性质。下列说法正确的是

A.①中固体可换为 NH4Cl
B.②中药品为 P2O5
C.反应一段时间后,③中黑色固体变为红色
D.反应一段时间后,④中锥形瓶收集到液氨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中国在南极建设的第四个科学考察站——泰山站。为了延长科学考察站基础设施使用寿命,钢铁设备表面镶嵌一些金属块(M)。下列说法正确的是

A. 金属块M可能是铜,发生氧化反应
B. 这种保护方法叫牺牲阳极的阴极保护法
C. 科考考察站里的设备在潮湿空气中主要发生化学腐蚀
D. 若采用外加电流的阴极保护法,设备与电源正极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Ba(OH)2和NaOH的混合稀溶液中通入足量的CO2气体,生成沉淀的物质的量(n)和通入CO2气体体积(V)的关系如下图所示,试回答:

(1)a点之前的反应的离子方程式为________________。
(2)a点到b点之间的反应的离子方程式是________________、________________。
(3)c点二氧化碳体积是________L。
(4)混合稀溶液中Ba(OH)2和NaOH的物质的量之比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,所含分子数相同的是( )
A.10g H2 和10g O2B.9g H2O 和0.5mol Br2
C.5.6L N2(非标准状况)和11g CO2D.224mLH2 (标准状况)和0.1mol N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近一期《物理评论快报》报道了科学家成功制备了包含钙(Ca)、钾(K)、铁(Fe)和砷(As)以及少量镍(Ni)的新型化合物材料[CaK(Fe1-x一Nix)4As4).回答下列问题:
(1)基态镍原子的价层电子排布式为________,基态砷原子最高能级的电子云有________个伸展方向.
(2)亚铁氰化钾{K4[Fe(CN)6]}是食盐中广泛使用的抗结剂,化学式中涉及的所有元素的笫一电离能由小到大的顺序为________,[Fe(CN)6]4-中,铁提供的空轨道数目为________,气态化合物X与CN一互为等电子体,则X的化学式为________.
(3)AsCl3分子中砷的杂化类型为________;其空间构型为________。
(4)已知:CaO、K2S的熔点分别为2572℃、840℃,二者熔点差异的主要原因是________。
(5)镍和硫形成的某晶体.其晶胞如图所示.巳知该晶体密度为dgcm-3,NA为阿伏加德罗常数的值。则Ni、S原子最短核间距(D)为________________cm。
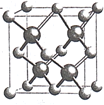
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着我国航天事业的飞速发展,对材料的需求也越来越多,聚芳酯(PAR)是分子主链上带来苯环和酯基的特种工程塑料,其结构简式为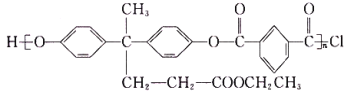 ,在航空航天等领域应用广泛。下图是利用乙酰丙酸(CH3COCH2CH2COOH)合成聚芳酯E的路线(省略部分产物):
,在航空航天等领域应用广泛。下图是利用乙酰丙酸(CH3COCH2CH2COOH)合成聚芳酯E的路线(省略部分产物):
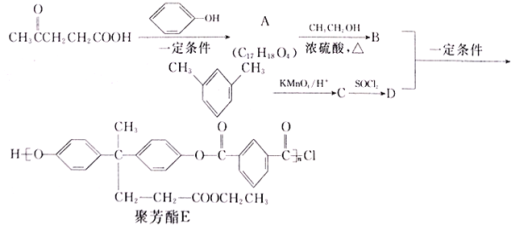
已知: 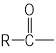 OH+SOCl2--→
OH+SOCl2--→ Cl+SO2 + HCl
Cl+SO2 + HCl
 Cl+R'OH→
Cl+R'OH→ OR'+HCl (R、R' 表示烃基)
OR'+HCl (R、R' 表示烃基)
(1)A中含有的官能团是_____________(填官能团名称)。
(2)A与CH3CH2OH反应生成B的反应类型为_____________________________。A的结构简式为________________________。
(3)写出B+D→E 的化学方程式为__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com