
科目:高中化学 来源:不详 题型:单选题
| 化学式 | AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 溶度积 | 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.5×10-16 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.25℃时,0.1 mol·L-1HF溶液中pH=1 | B.该体系中有CaF2沉淀产生 |
C.该体系中KSP(CaF2)=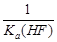 | D.KSP(CaF2)随温度和浓度的变化而变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
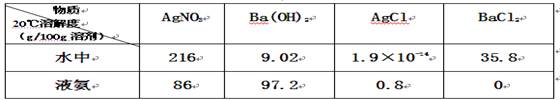
| A.2AgNO3+BaCl2=2AgCl↓+Ba(NO3)2 | B.2AgNO3+BaCl2=2AgCl+Ba(NO3)2↓ |
| C.2AgCl+Ba(NO3)2=2AgNO3↓+BaCl2 | D.2AgCl+Ba(NO3)2=2AgNO3+BaCl2↓ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.AgCl不溶于水,不能转化为AgI |
| B.两种不溶物的Ksp相差越大,不溶物就越容易转化为更难溶的不溶物 |
| C.AgI比AgCl更难溶于水,所以AgCl可以转化为AgI |
| D.常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将AlCl3溶液蒸干并灼烧后得到的物质是Al(OH)3 |
| B.向饱和AgCl水溶液中加入盐酸,Ksp值变大 |
| C.温度一定时,当溶液中Ag+和Cl-浓度的乘积等于Ksp值时,此溶液为AgCl的饱和溶液 |
| D.所谓沉淀完全就是用沉淀剂将溶液中某一离子除净; |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.BaSO4溶解度增大,Ksp不变 |
| B.BaSO4溶解度、Ksp均增大 |
| C.BaSO4溶解度不变,Ksp增大 |
| D.BaSO4溶解度、Ksp均不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溶液的质量 | B.Ca(OH)2的溶解度 |
| C.溶液中Ca2+离子的数目 | D.溶液中溶质的质量分数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com