
【题目】氮元素可以形成多种物质,根据已学的知识,回答下列问题:
(1)氮原子的核外电子排布式是___________,其最外层电子有_____种不同的运动状态。
(2)氮气在常温常压下是很稳定的,对此的合理解释是____________________。
(3)N元素处于同一主族的P、As元素,这三种元素形成的气态氢化物的稳定性由大到小的顺序是________________________。
(4)工业上常用氮气与氢气来合成氨气,温度控制在400~500 ℃,采用铁触媒做催化剂,压强控制在2 ⅹ 105 ~ 5 ⅹ 105 Pa。
①该反应的化学方程式为_____________________。
它的平衡常数表达式为_______________________。
②在一体积为10 L的密闭容器中充入了280 g N2,100 g H2,反应半小时后,测得有34 g NH3生成,则用H2表示该反应的速率为_________mol/(Lmin)。此时,氮气的转化率为__________。
③下列判断可以作为该反应达到平衡的标志的是(_______)
A.单位时间内每消耗1摩尔氮气的同时消耗3摩尔氢气
B.混合气体的平均分子量不再发生变化
C.混合气体的密度保持不变
D.体系的温度不再变化
④当反应达到平衡后的t2时刻,将混合气体通过“分子筛”,可以及时将产物NH3分理出平衡体系,这会使得平衡正向移动,请根据平衡移动原理,在下图中画出t2时刻后平衡移动的示意图:_____________

⑤当及时分离出氨气后,工业上常常将氮气、氢气再次转移到反应器,这样做的原因是________________。
⑥氨气常用来生产化肥NH4Cl,NH4Cl溶于水会使得溶液显__________性,在该盐的水溶液中存在多种微粒:NH4+、NH3H2O、H+、Ci-,这些离子浓度由大到小的顺序为_________;该盐溶液中还存在多种守恒,请任意写出一种合理的守恒关系式___________________。
⑦工业上常用氨气来制备硝酸,其中第1步是用氨气与纯氧在Cr2O3的催化作用下制得NO和水。请写出这个反应的化学方程式并配平______________________。该反应中,还原剂是_________________,若反应中转移了1.204 ⅹ 1024 个电子,则生成的 NO在标准状况下的体积是________L。
【答案】 1s22s22p3 5 氮气分子中存在叁健 NH3 > PH3 > AsH3 N2 + 3H2 = 2NH3 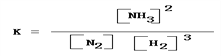 0.01 mol/(Lmin) 10% BD
0.01 mol/(Lmin) 10% BD 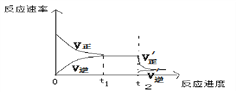 提高原料N2、H2的利用率,降低生产成本 酸性 [ Cl-] 〉[NH4+] 〉[H+] 〉[NH3H2O] [H+] + [NH4+] = [OH-] + [Cl-] 或 [Cl-] = [NH3H2O]+ [NH4+]或 [H+] = [OH-] + [NH3H2O] 4 NH3 + 5O2
提高原料N2、H2的利用率,降低生产成本 酸性 [ Cl-] 〉[NH4+] 〉[H+] 〉[NH3H2O] [H+] + [NH4+] = [OH-] + [Cl-] 或 [Cl-] = [NH3H2O]+ [NH4+]或 [H+] = [OH-] + [NH3H2O] 4 NH3 + 5O2 ![]() 4NO + 6H2O NH3 8.96 L
4NO + 6H2O NH3 8.96 L
【解析】(1)氮元素的核电荷数为7,基态氮原子的核外电子排布式是 1s22s22p3,其最外层电子数为5,有5种不同的运动状态;
(2)氮气分子中存在叁健,导致氮气在常温常压下化学性质很稳定;
(3)非金属性越强形成的气态氢化物的稳定性越强,N、P、As元素的非金属性随核电荷数增大而减小,则三种元素形成的气态氢化物的稳定性由大到小的顺序是NH3>PH3>AsH3 ;
(4) ①合成氨反应的化学方程式为N2 + 3H2 ![]() 2NH3;此反应的平衡常数表达式为
2NH3;此反应的平衡常数表达式为![]() ;
;
②在一体积为10 L的密闭容器中充入![]() =10molN2,
=10molN2, ![]() =50molH2,反应半小时后,测得有
=50molH2,反应半小时后,测得有![]() =2molNH3生成,则用H2表示该反应的速率为
=2molNH3生成,则用H2表示该反应的速率为![]() ×
×![]() mol/(Lmin)=0.01 mol/(Lmin);此时,氮气的转化率为
mol/(Lmin)=0.01 mol/(Lmin);此时,氮气的转化率为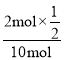 ×100%=10%;
×100%=10%;
③A.单位时间内每消耗1摩尔氮气的同时消耗3摩尔氢气,均为正反应速率,无法判断是平衡状态,故A错误;B.混合气体的质量始终不变,混合气体的总物质的量是不定值,混合气体的平均分子量不再发生变化,说明反应达到平衡,故B正确;C.混合气体的质量和体积始终不变,密度保持不变,无法说明是平衡状态,故C错误;D.体系的温度不再变化,说明反应处于相对静止状态,是平衡状态,故D正确;答案为BD;
④平衡后将NH3分离出平衡体系,即减小生成物的浓度,逆反应速率瞬间减小,正反应速率瞬间不变,平衡正向移动,重新形成新的平衡状态,t2时刻后平衡移动的示意图为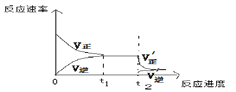 ;
;
⑤将反应后的氮气、氢气再次转移到反应器,这样做提高原料N2、H2的利用率,降低生产成本;
⑥NH4Cl溶于水,NH4+的水解会使得溶液显酸性,在该盐的水溶液中存在多种微粒:NH4+、NH3H2O、H+、Cl-,其中NH3H2O是水解产物,H+来源于水和NH4+的水解,
则离子浓度由大到小的顺序为[ Cl-] 〉[NH4+] 〉[H+] 〉[NH
⑦氨气与纯氧在Cr2O3的催化作用下制得NO和水,根据电子守恒及原子守恒得此反应的化学方程式4 NH3 + 5O2 ![]() 4NO + 6H2O,该反应中,氨气中氮元素化合价升高,发生氧化反应,氨气是还原剂,若反应中转移了1.204×1024个电子,即转移2mol电子,参加反应的NH3的物质的量为
4NO + 6H2O,该反应中,氨气中氮元素化合价升高,发生氧化反应,氨气是还原剂,若反应中转移了1.204×1024个电子,即转移2mol电子,参加反应的NH3的物质的量为![]() =0.4mol,生成NO的物质的量为0.4mol, NO在标准状况下的体积是0.4mol×22.4L/mol=8.96L。
=0.4mol,生成NO的物质的量为0.4mol, NO在标准状况下的体积是0.4mol×22.4L/mol=8.96L。


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
【题目】观察下面列出的几种物质的化学式或者结构式(填序号)
①![]() ②
②![]() ③CH3CH2CH3 ④CH3CH2CH2CH3
③CH3CH2CH3 ④CH3CH2CH2CH3
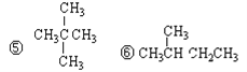
⑦H2 ⑧D2 ⑨O2 ⑩O3
(1)互为同分异构体的是____________________________;
(2)互为同系物的是________________________________;
(3)互为同位素的是________________________________;
(4)互为同素异形体的是____________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有两种有机物Q(![]() )与P(
)与P(![]() ),下列有关它们的说法中正确的是( )
),下列有关它们的说法中正确的是( )
A. 二者的核磁共振氢谱中均只出现两种峰且峰面积之比为3∶2
B. 二者在NaOH醇溶液中均可发生消去反应
C. 一定条件下,二者在NaOH溶液中均可发生取代反应
D. Q的一氯代物只有1种、P的一溴代物有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】迷迭香酸是从蜂花属植物中提取得到的酸性物质,迷迭香酸的分子结构如图,下列叙述正确的是( )

A.迷迭香酸属于芳香族化合物,分子式C18H18O8
B.迷迭香酸含有碳碳双键、羟基、羧基、苯环和酯基的结构
C.1mol迷迭香酸最多能和含6mol Br2的浓溴水发生反应
D.1mol迷迭香酸最多与含5mol NaOH的水溶液完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,不属于化学变化的是( )
A.鲜花通入氯气后褪色了
B.淀粉KI试纸滴加溴水后变蓝
C.胶体和溶液可以通过半透膜进行渗析分离
D.过氧化钠使某些染料褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把一定量的铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+与 Fe3+的物质的量浓度之比为3∶2。则已反应的Fe3+与未反应的Fe3+的物质的量之比是( )
A. 1∶1 B. 1∶2 C. 2∶1 D. 2∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 按分散剂种类可将分散系分为溶液、胶体和浊液
B. 水玻璃、碘水、Fe(OH)3胶体均为混合物
C. CO2、SO3、CO均属于酸性氧化物
D. KNO3溶液、Cu、熔融的NaCl均能导电,所以它们都属于电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况,试判断哪些违反了泡利原理__________,哪些违反了洪特规则__________。

(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为__________;其最高价氧化物对应水化物的化学式是__________。
(3)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列。
①2s ②3d ③4s ④3s ⑤4p ⑥3p
轨道能量由低到高排列顺序是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com