
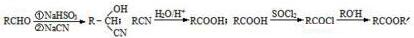
 .
. $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$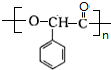 +nH2O.
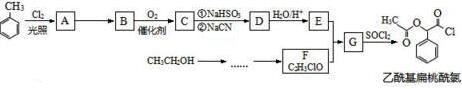
+nH2O.分析 根据题中各物质转化关系,结合题中信息可知,甲苯在光照条件下与氯气反应生成A为 ,A发生碱性水解得B为
,A发生碱性水解得B为 ,B发生氧化反应得C为
,B发生氧化反应得C为 ,C发生信息中的反应得D为
,C发生信息中的反应得D为 ,D酸性水解得E为
,D酸性水解得E为 ,根据F的分子式可知,乙醇氧化成乙酸,乙酸再与SOCl2发生信息中的反应生成F为CH3COCl,F和E发生取代反应生成G为
,根据F的分子式可知,乙醇氧化成乙酸,乙酸再与SOCl2发生信息中的反应生成F为CH3COCl,F和E发生取代反应生成G为 ,G与SOCl2反应生成乙酰基扁桃酰氯,据此答题.
,G与SOCl2反应生成乙酰基扁桃酰氯,据此答题.
解答 解:根据题中各物质转化关系,结合题中信息可知,甲苯在光照条件下与氯气反应生成A为 ,A发生碱性水解得B为
,A发生碱性水解得B为 ,B发生氧化反应得C为
,B发生氧化反应得C为 ,C发生信息中的反应得D为
,C发生信息中的反应得D为 ,D酸性水解得E为
,D酸性水解得E为 ,根据F的分子式可知,乙醇氧化成乙酸,乙酸再与SOCl2发生信息中的反应生成F为CH3COCl,F和E发生取代反应生成G为
,根据F的分子式可知,乙醇氧化成乙酸,乙酸再与SOCl2发生信息中的反应生成F为CH3COCl,F和E发生取代反应生成G为 ,G与SOCl2反应生成乙酰基扁桃酰氯,
,G与SOCl2反应生成乙酰基扁桃酰氯,
(1)根据上面的分析可知,A→B反应所需的试剂及条件为氢氧化钠水溶液、加热,
故答案为:氢氧化钠水溶液、加热;
(2)根据上面的分析可知,D的结构简式 为 ,
,
故答案为: ;
;
(3)E为 ,E发生缩聚反应生成高分子聚合物,反应方程式为n
,E发生缩聚反应生成高分子聚合物,反应方程式为n $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$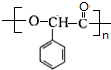 +nH2O,
+nH2O,
故答案为:n $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +nH2O;
+nH2O;
(4)根据乙酰基扁桃酰氯的结构简式可知,有5种不同化学环境的氢原子,
故答案为:5;
(5)以乙醇为原料制备F,可以用乙醇氧化成乙酸,乙酸再与SOCl2发生信息中的反应生成F为CH3COCl,反应的合成路线为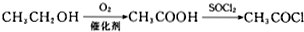 ,
,
故答案为: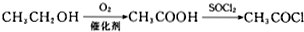 .
.
点评 本题主要考查的是有机物的合成与有机物的推断,充分掌握常见有机化合物的性质以及抓住所给信息解题是关键,难度中等,注意有机官能团的性质的灵活运用.


科目:高中化学 来源: 题型:解答题
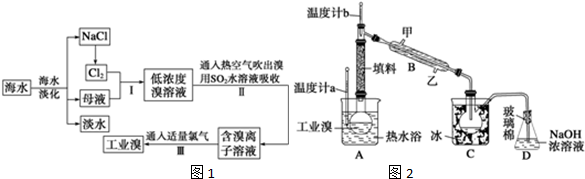
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠保存在煤油中 | |
| B. | 白磷保存在水中 | |
| C. | 在FeCl3 溶液中加入一定量铁粉,防止溶液变质 | |
| D. | 为了检验FeCl2溶液是否变质,可用KSCN 溶液检验 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1的(NH4)2Fe(SO4)2•6H2O溶液中:c(NH4+)=c(SO42-)>c(Fe2+)>c(H+) | |
| B. | 等pH的①(NH4)2SO4溶液 ②NH4HSO4溶液 ③NH4Cl溶液中,c(NH4+)的大小关系:①>③>② | |
| C. | 0.1 mol•L-1的NaHCO3溶液:c(Na+)>c(OH-)>c(HCO3-)>c(H+) | |
| D. | 标准状况下将2.24L CO2气体通入150mL 1mol•L-1的NaOH溶液中,充分反应后溶液中c(HCO3-)>c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤ | B. | ④⑤ | C. | ②③ | D. | ⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.7mol Na2O2与足量的CO2气体反应,电子转移0.7NA | |
| B. | 足量水蒸气与16.8gFe粉反应转移0.9mol电子 | |
| C. | Na与水、Al与NaOH溶液反应中水均作氧化剂 | |
| D. | 用钠从四氯化钛中置换钛,利用了钠的强还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com