
在无色酸性溶液中,下列离子能大量共存的是
A.Na+ 、NH4+ 、NO3-、SO32- B.Mg2+、SO42-、K +、Cl-
C.K + 、Cu2+ 、Cl-、Br- D.Ba2+ 、Na+ 、OH-、HCO3-
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案科目:高中化学 来源: 题型:
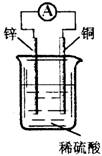
关于右图所示装置的说法中,不正确的是
A.铜片上发生氧化反应
B.电子由锌片通过导线流向铜片
C.该装置能将化学能转化为电能
D.锌片是该装置的负极,该电极反应为Zn—2e—==Zn2+
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在实验室,可以用如图7所示的装置制取乙酸乙酯。请回答下列问题:
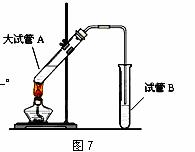
(1)左侧试管中需加浓硫酸做 ▲ 和吸水剂,
右侧试管中盛放的试剂是 ▲ ,
右侧导气管的下端不能插入液面以下,其目的是 ▲ 。
(2)写出实验室用乙醇和乙酸制取乙酸乙酯的化学反应方程式
▲ 。
(3)该反应是典型的可逆反应,若不把生成的乙酸乙酯及时蒸馏 出来,反应一段时间后,
就会达到化学平衡状态。下列能说明该反应已达到化学平衡状态的有(填序号) ▲ 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水;
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸;
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸;
④混合物中各物质的浓度不再变化。
(4)若现有乙酸 90g、乙醇138g发生酯化反应得到66 g乙酸乙酯,试计算该反应的产率为 ▲ 。(产率指的是某种生成物的实际产量与理论产量的比值)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知正己烷的球棍模型为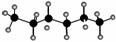 。某有机物a的分子式和正己烷相同,且主链上有4个碳原子,则下列关于a的观点正确的是 ( )。
。某有机物a的分子式和正己烷相同,且主链上有4个碳原子,则下列关于a的观点正确的是 ( )。
A.a分子中可能有三个甲 基
基
B.a的分子式为C6H10
C.a的一氯代物可能有三种
D.在光照条件下,a能与溴的四氯化碳溶液发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
在中国,珊瑚是吉祥富有的象征,台湾的红珊瑚尤其珍贵。其是无数珊瑚虫分泌的石灰质大量堆积形成的干支状物,呈红色是因为在海底长期积淀某种元素的化合物导致的,该元素是
A.Na B.Fe C.Si D.Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2FeO4是一种高效多功能水处理剂,应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4 + 6Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,对此反应下列说法中正确的是
A.Na2O2只作氧化剂 B.FeSO4只作还原剂
C.铁元素被还原
D.2 mol FeSO4发生反应时,反应中共有8 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]是分析化学中重要的试剂,常用于代替硫酸亚铁。
已知:硫酸亚铁铵在 500℃时隔绝空气加热完全分解,发生了氧化还原反应,(1)固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO3、H2O、N2和 (填写化学式)
实验:为检验分解产物的成份,设计如下实验装置进行实验,加热A中的硫酸亚铁铵至分解完全。
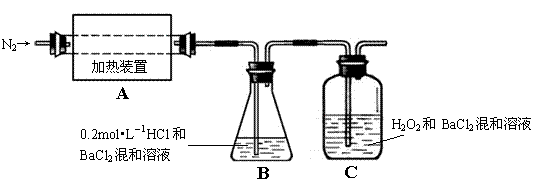
(2)A中固体充分加热较长时间后,通入氮气,目的是
(3)为验证A中残留物是否含有FeO,需要选用的试剂有
A.KSCN溶液 B.浓盐酸 C.KMnO4溶液 D.稀硫酸
(4)装置B中BaCl2溶液的作用是为了检验分解产物中是否有 气体生成,若含有该气体,观察到的现象为
(5)现欲将B中溶液准确稀释至100.00mL,应将锥形瓶中的溶液转移入
(填仪器名称)定容。实验中,观察到C中有白色沉淀生成,则C中发生的反应为 (用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
电池是人类生产和生活中的重要能量,各式各样电池的发明是化学对人类的一项重大贡献,下列有关电池的叙述正确的是( )
A.锌锰干电池工作一段时间后碳棒变细
B.氢氧燃料电池可将热能直接转变为电能
C.氢氧燃料电池工作时氢气在负极被氧化
D.太阳能电池的主要材料是高纯度的二氧化硅
查看答案和解析>>
科目:高中化学 来源: 题型:
Fe2+和Fe3+可以互相转化,现提供的物质有FeCl2溶液、FeCl3溶液、Fe粉、
KSCN溶液、3%H2O2,请你完成实验报告证明Fe2+和Fe3+的互相转化。
| 实 验 步 骤 | 实 验 现 象 | 结 论 |
| 1.①将KSCN溶液滴入盛有FeCl2溶液的试管中,充分振荡 ②再滴入______________,充分振荡 | ①__________________ ②溶液变红 | Fe2+被Cl2氧化成 Fe3+ |
| 2.①在盛有足量Fe粉的试管中滴入FeCl3溶液,充分振荡 ②再滴入KSCN溶液,充分振荡 | ①溶液由___________色变为___________色 ②无明显现象 | __________________________ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com