
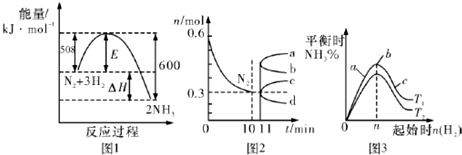
| A. | 升高温度,该反应的平衡常数增大 | |
| B. | 由图2信息,10 min内该反应的平均速率v(H2)=0.09 mol•L-1•min-1 | |
| C. | 由图2信息,从11 min起其它条件不变,压缩容器的体积,则n(N2)的变化曲线为d | |
| D. | 图3中温度T1<T2,a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是b点 |
分析 A.由图可知,反应物总能量大于生成物总能量,该反应为放热反应;
B.10 min内该反应的平均速率v(N2)=$\frac{\frac{0.6mol-0.3mol}{2L}}{10min}$=0.015 mol•L-1•min-1,结合速率之比等于化学计量数之比计算;
C.从11 min起其它条件不变,压缩容器的体积,平衡正向移动,n(N2)减小;
D.a、b、c三点均在同一曲线上,氢气的物质的量越大,氮气的转化率越大.
解答 解:A.由图可知,反应物总能量大于生成物总能量,该反应为放热反应,则升高温度,平衡逆向移动,平衡常数K减小,故A错误;
B.10 min内该反应的平均速率v(N2)=$\frac{\frac{0.6mol-0.3mol}{2L}}{10min}$=0.015 mol•L-1•min-1,由速率之比等于化学计量数之比可知,v(H2)=0.045 mol•L-1•min-1,故B错误;
C.从11 min起其它条件不变,压缩容器的体积,平衡正向移动,n(N2)减小,可知n(N2)的变化曲线为d,故C正确;
D.温度、体积不变时,氢气的物质的量越大,氮气的转化率越大,a、b、c三点均在同一曲线上,均为平衡状态点,则反应物N2的转化率最高的是c点,故D错误;
故选C.
点评 本题考查物质的量随时间的变化曲线、反应热与焓变,为高频考点,把握图象分析、反应中能量变化、平衡移动为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | CuO、Na2O和Na2O2都是碱性氧化物 | |
| B. | SO2能与碱反应生成盐和水,因此SO2属于酸性氧化物 | |
| C. | NH4Cl不含金属阳离子,不属于盐 | |
| D. | 金属氧化物都是碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
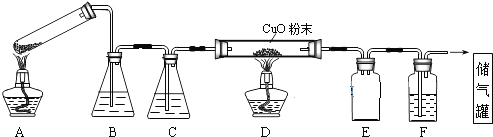
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
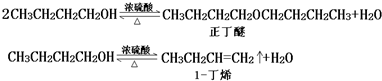
| 化合物 | 密度(g•cm-3) | 水溶性 | 沸点(℃) |
| 冰乙酸 | 1.05 | 易溶 | 118.1 |
| 正丁醇 | 0.80 | 微溶 | 117.2 |
| 正丁醚 | 0.77 | 不溶 | 142.0 |
| 乙酸正丁酯 | 0.90 | 微溶 | 126.5 |
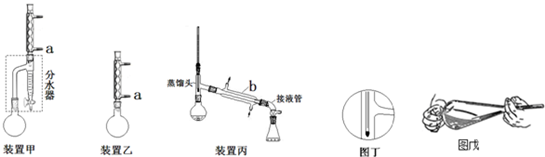

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
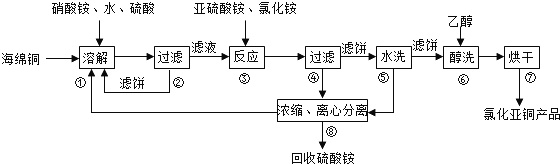
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线:
苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线: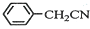 +H2O+H2SO4$\stackrel{100~130℃}{→}$
+H2O+H2SO4$\stackrel{100~130℃}{→}$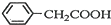 +NH4HSO4
+NH4HSO4 +Cu(OH)2→(
+Cu(OH)2→(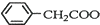 )2Cu+H2O
)2Cu+H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铷比镁金属性强 | |
| B. | 氯化镁比氯化铷难溶 | |
| C. | 高温下,镁离子得电子能力比铷离子弱 | |
| D. | 铷的沸点比镁低,当把铷蒸气抽走时,平衡向右反应方向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com