
【题目】黄铜矿不仅可用于火法炼铜,也可用于湿法炼铜,湿法可同时生产铜、磁性氧化铁和用于橡胶工业的一种固体物质A,流程如下:
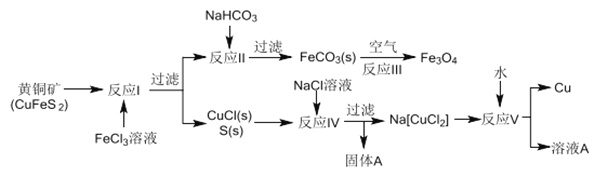
(1)黄铜矿中Cu 的化合价是______,反应I中65gFeC13 可氧化________mol CuFeS2。
(2)工业生产中的过滤操作多采用倾析法分离出固体物质,下列适合用倾析法的有______。
A.沉淀的颗粒较大 B.沉淀容易沉降 C.沉淀呈胶状 D.沉淀呈絮状
(3)在反应Ⅱ中,计算NaHCO3饱和溶液(其中CO32-平衡浓度为1.2×10-3mol/L)可产生FeCO3沉淀时的最小Fe2+浓度是_________(己知FeCO3的Ksp=3.0×10-11)
(4)反应Ⅲ是在设备底部鼓入空气,高温氧化锻烧法来制备磁性氧化铁,写出对应的化学方程式_________________。
(5)固体物质A的成分________(写名称)。
(6)潮湿的FeCO3固体若不及时灼烧处理会在空气中逐渐变红,写出相关的化学方程式:_______________。
(7)本流程中可实现循环使用的物质除了水外,还有_____________
【答案】 +2 0.1 AB 2.5×10-8mol/L 6FeCO3+O2![]() 2Fe3O4+6CO2 硫 6FeCO3+O2+6H2O==4Fe(OH)3+4CO2 氯化钠
2Fe3O4+6CO2 硫 6FeCO3+O2+6H2O==4Fe(OH)3+4CO2 氯化钠
【解析】 (1)根据化合价的代数和为0,黄铜矿CuFeS2中Cu 的化合价为+2价,Fe为+2价,S为-2价;65gFeC13 的物质的量为![]() =0.4mol,反应后得到0.4mol电子,根据流程图,反应后生成CuCl和S,只有S元素被氧化,根据得失电子守恒,能够氧化0.1mol CuFeS2,故答案为:+2;0.1;
=0.4mol,反应后得到0.4mol电子,根据流程图,反应后生成CuCl和S,只有S元素被氧化,根据得失电子守恒,能够氧化0.1mol CuFeS2,故答案为:+2;0.1;
(2) 沉淀的颗粒较大,静止后容易沉降至容器底部,常用倾析法分离,沉淀呈胶状或絮状,静止后不容易沉降,不能采取倾析法分离,故选AB;
(3)在反应Ⅱ中, NaHCO3饱和溶液中CO32-平衡浓度为1.2×10-3mol/L,可产生FeCO3沉淀时的最小Fe2+浓度为 =
=![]() =2.5×10-8mol/L,故答案为:2.5×10-8mol/L;
=2.5×10-8mol/L,故答案为:2.5×10-8mol/L;
(4)反应Ⅲ中,在设备底部鼓入空气,碳酸亚铁被氧化生成磁性氧化铁(Fe3O4),反应的化学方程式为6FeCO3+O2![]() 2Fe3O4+6CO2,故答案为:6FeCO3+O2
2Fe3O4+6CO2,故答案为:6FeCO3+O2![]() 2Fe3O4+6CO2;
2Fe3O4+6CO2;
(5)根据流程图,加入氯化钠溶液将CuCl转化为络合物,固体物质A为硫,故答案为:硫;
(6)亚铁离子具有还原性,在潮湿的空气中FeCO3固体被氧化变红,反应的化学方程式6FeCO3+O2+6H2O==4Fe(OH)3+4CO2,故答案为:6FeCO3+O2+6H2O==4Fe(OH)3+4CO2;
(7)根据流程图,溶液A中含有氯化钠,可以参与循环使用,故答案为:氯化钠。


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】
第一步:配制饱和NaCl溶液,倒入烧杯中加热;
第一步:控制温度在30-35 ℃。边搅拌边分批加入研细的NH4HCO3固体,加料完毕后,继续保温30分钟;
第三步:静置、过滤得NaHCO3晶体.用少量蒸馏水洗涤除去杂质,然后抽干;
第四步:将第二步所得固体转入蒸发皿中,灼烧2小时,制得纯碱固体,
已知:温度高于35℃时,NH4HCO3会分解。有关盐的溶解度(g/100g水)如下表:
盐 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | —— | —— | —— | —— |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.l | 12.7 | 14.5 | 16.4 | —— |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
回答下列问题:
(1)反应温度控制在30-35℃范围内,应采取的加热方法为 ,反应温度不能高于35℃的理由是 .
(2)第三步静置后析出NaHCO3晶体的原因是 ;用蒸馏水洗涤NaHCO3晶体的目的是除去杂质粒子 (用离子符号表示)。
(3)若向过滤所得母液中加入 (填写试剂名称),并作进一步处理,使NaCl溶液循环使用,同时可回收NH4Cl。
(4)纯碱产品不纯,含有NaHCO3、NaCl等杂质。测定纯碱中NaHCO3含量的方法是:准确称取纯碱样品Wg,放入锥形瓶中加蒸馏水溶解,加l-2滴酚酞指示剂,用物质的量浓度为cmol/L的盐酸滴定至溶液由红色到无色(指示CO32-+H+=HCO3-反应的终点), 所用盐酸体积为V1mL,再加1-2滴甲基橙指示剂,继续用盐酸滴定至溶液由黄变橙,所用盐酸总体积为V2mL。
① 实验室配制一定体积cmol/L盐酸需用的仪器除了容量瓶、烧杯、量筒外还需 ;在容量瓶的使用方法中,下列操作正确的是 (填写标号)
a.使用容量瓶前检验它是否漏水
b.容量瓶用蒸馏水洗净后,再用待配溶液润洗
c.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中.然后加蒸馏水定容
d.用容量瓶把溶液配制完成以后.直接贴上标签,放置备用
e.定容后盖好瓶塞,用食指顶住瓶塞,用另一只手指托住瓶底,把容量瓶倒转和摇动几次
② 写出纯碱样品中NaHCO3质量分数的计算式:NaHCO3(%)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的相对位置如下表所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。

请回答下列问题:
(1)元素X在周期表中的位置为________。
(2)最高价氧化物对应的水化物的浓溶液与其氢化物能发生氧化还原反应的元素是________(写元素符号)。
(3)XW2的电子式为________。
(4)Z的最高价氧化物对应的水化物的化学式为________。
(5)W和Y形成的一种二元化合物具有色温效应,其相对分子质量在170-190之间,且W的质量分数约为70%,该化合物的化学式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 棉花和蚕丝的主要成分都是纤维素
B. 蛋白质在一定条件发生水解反应生成葡萄糖
C. 煤的气化是在高温下煤和水蒸气作用转化为可燃性气体的过程
D. 食用植物油的主要成分是不饱和高级脂肪酸甘油酯,属于高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对化学反应的认识错误的是 ( )
A.有化学键破坏的一定是化学反应 B.会产生新的物质
C.可能会引起物质状态的变化 D.一定伴随着能量的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如右图所示的原电池,下列说法正确的是( )。

A.电流从锌电极通过电流表流向铜电极
B.锌电极发生还原反应,铜电极发生氧化反应
C.当有13 g Zn溶解时,外电路中就有0.4 mol电子通过
D.铜电极作正极,发生的电极反应为2H++2e-===H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋硝香豆素是一种治疗心脑血管疾病的药物,能阻碍血栓扩展,其结构简式为: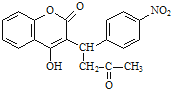 ,醋硝香豆素可以通过以下方法合成(部分反应条件省略)。
,醋硝香豆素可以通过以下方法合成(部分反应条件省略)。
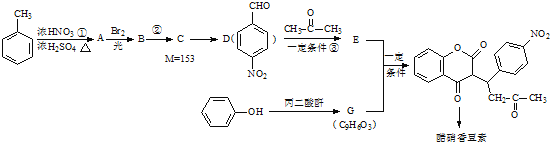
已知: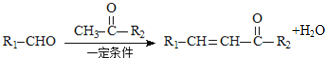
回答以下问题:
(1)反应①的反应类型是_____________。
(2)D为的名称是________,其在水中的溶解度________(填“大”或“小”)。
(3)反应②的条件是_________。
(4)反应③的化学方程式为___________。
(5)关于E物质,下列说法正确的是__________(填序号)。
a. 可以发生加成反应、聚合反应、氧化反应和还原反应
b. 在核磁共振氢谱中有四组吸收峰
c. 可以用酸性高锰酸钾溶液鉴别D和E
d. 存在顺反结构
(6)分子结构中只含有一个环,且同时符合下列条件的B的同分异构体共有______种。
①能与碳酸氢钠反应生成气体,又能与盐酸反应生成类似于铵盐的物质
②苯环上有三个取代基
(7)已知有机酸酐是二个羧基脱一分子水,例如乙酸酐就是二分子乙酸脱掉一分子水,结构简式为(CH3CO)2O,请写出苯酚和丙二酸酐生成G的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 钠和钾的合金可用于快中子反应堆作热交换剂
B. 可用超纯硅制造的单晶硅来制芯片
C. 可利用二氧化碳制造全降解塑料
D. 氯气有毒,不能用于药物的合成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com