
某同学通过系列实验探究Mg及其化合物的性质, 操作正确且能达到目的的是
操作正确且能达到目的的是
A、将水加入浓硫酸中得到稀硫酸,置镁片于其中探究讨Mg的活泼性
B、将NaOH溶液缓慢滴入MgSO4溶液中,观察Mg(OH)2沉淀的生成
C 、将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀
、将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀
D、将Mg(OH)2沉淀转入表面皿中,加足量稀盐酸,加热蒸干得无水MgCl2固体
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
A、B、C、D为原子序数依次增大的前四周期元素,元素A基态原子核外有3个未成对电子,元素B原子最外层电子数是内层电子数的3倍,元素C的最高价和最低价代数和等于0,元素D位于周期表ⅥB族。
(1)判断离子AB 的空间构型为________。
的空间构型为________。
(2)元素A、C形成的化合物熔点高,但比B、C形成的化合物熔点低,其原因是 。
 (3)在A的氢化物(A2H4)分子中,A原子轨道的杂化类型是________。
(3)在A的氢化物(A2H4)分子中,A原子轨道的杂化类型是________。
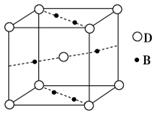
(4)元素B与D形成的一种化合物广泛应用于录音磁带上,
其晶胞如右图所示。该化合物的化学式为________。
(5)向D的氯化物DCl3溶液中滴加氨水可形成配合Cl
①D原子的外围电子排布式为________。
②1 mol该配合物中含配位键的数目为________。
(6) D元素以D2O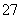 的形式存在于酸性废水中,常用FeSO4将其还原为D3+,写出该反应的离子方程式为___________________________________________。
的形式存在于酸性废水中,常用FeSO4将其还原为D3+,写出该反应的离子方程式为___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
反应A+3B=2C+2D在不同条件下反应速率如下,其中最快的是( )
|
| A. | v(A)=0.15mol/(L•min) | B. | v(B)=0.6mol/(L•min) |
|
| C. | v(C)=0.4mol/(L•min) | D. | v(D)=0.0075 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的短周期部分,表中字母分别表示一种元素.

请回答下列问题:
(1)g与b可形成离子化合物b2g2,该物质含有的化学键类型有 .
(2)e、f、g三种元素气态氢化物的稳定性由弱到强的顺序为(用化学式表示) .
(3)从化合物c2g3与eg2组成的混合物中分离提纯eg2,可加入上述 (用元素符号表示)两种元素形成化合物的水溶液后再过滤洗涤.
(4)a、d两种元素可形成多种化合物,其中化合物X的产量是衡量一个国家石油化工发展水平的标志.X可与H2O在一定条件下反应生成化合物A,该反应的化学方程式为: .
(5)航天技术中常使用a和g单质组成的燃料电池,该电池具有高能、轻便和不污染环境等优点.该电池反应为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
是制取航天航空工业材料——钛合金的重要原料。由钛铁矿(主要成分是FeTiO3)制备TiCl4等产品的一种工艺流程示意如下:
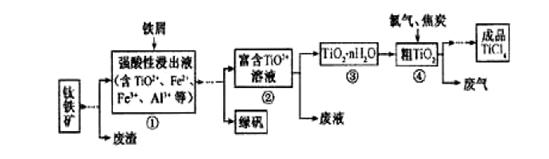
回答下列问题:
(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生:
2Fe3++Fe === 3Fe2+
2TiO2+(无色) +Fe+4H+ === 2Ti3+(紫色) +Fe2++2H2O
Ti3+(紫色) +Fe3++H2O === TiO2+(无色) +Fe2++2H+
加入铁屑的作用是____________。
(2)在②→③工艺中需要控制条件以形成TiO2·n H2O溶胶,该分散质颗粒直径大小在_____________范围。
(3)若把③中制得的固体TiO2·n H2O用酸清洗除去其中的Fe (OH)3杂质,还可制得钛白粉。已知25℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe (OH)3+3H+ Fe3+ +H2O的
Fe3+ +H2O的 平衡常数K=_____________。
平衡常数K=_____________。
(4)已知:TiO2 (s) +2 Cl2 (g)=== TiCl4(l) +O2(g) △H=+140KJ·mol-1
2C(s) +O2(g)=== 2CO(g) △H=—221KJ·mol-1
写出④中TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热化学方程式:_____________。
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是_____________(只要求写出一项)。
(6)依据下表信息,要精制含少量SiCl4杂质的TiCl4 ,可采用_____________方法。
| TiCl4 | SiCl4 | |
| 熔点/℃ | -25.0 | -68.8 |
| 沸点/℃ | 136.4 | 57.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
C和Si元素在化学中占有极其重要的地位。
(1)写出Si的基态原子核外电子排布式______________。从电负性角度分析,C、Si和O元素的非金属活泼性由强至弱的顺序为______________。
(2)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为______________,微粒间存在的作用力是______________。
(3)氧化物MO的电子总数与SiC的相等,则M为______________(填元素符号)。MO是优良的耐高温材料,其晶体结构与NaCl晶体相似。MO的熔点比CaO的高,其原因是_________________________。
(4)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同。CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键。从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π键。___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
等量镁铝合金粉末分别与下列4种过量的溶液充分反应,放出氢气最多的是
A.2 mol·L-1 H2SO4溶液
B.18 mol·L-1 H2SO4溶液
C.6 mol·L-1 KOH溶液
D.3 mol·L-1 HNO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com