
���� ��֪A��B��C��D����ѧ��ѧ�ij������ʣ���A��B��C������ͬһ��Ԫ�أ�
��1����A����������ˮ������ӦΪCl2��D�����������������������;���Ľ������ʣ�ӦΪFe����BΪFeCl3��CΪFeCl2��
��2�������A��Ԫ���ǵؿ��к�������Ԫ�أ���AΪO��C�ڸ�¯�����еIJμ���Ҫ��Ӧ����CΪCO������BΪCO2��DΪC��
��3����A�ǵ���ɫ���壬D��������Ԫ����ɵ���ɫ��ζ���壬��AΪNa2O2��DΪCO2��BΪNa2CO3��CΪNaHCO3��
��4����B��CΪ�����Bת��ΪCʱ����������25%����AӦΪS��BΪSO2��CΪSO3��DΪO2��
��5����DΪǿ�������Һ��A��C����Һ�з�Ӧ���ɰ�ɫ����B����AΪƫ�����Σ�BΪ����������CΪ���Σ�DΪǿ�ᣬ��AΪ���Σ�BΪ����������CΪƫ�����Σ�DΪǿ����˴��⣮
��� �⣺��֪A��B��C��D����ѧ��ѧ�ij������ʣ���A��B��C������ͬһ��Ԫ�أ�
��1����A����������ˮ������ӦΪCl2��D�����������������������;���Ľ������ʣ�ӦΪFe����BΪFeCl3��CΪFeCl2��Cת��ΪB�����ӷ���ʽΪ2Fe2++Cl2=2Fe2++2Cl������A��Ư�۵Ļ�ѧ����ʽΪ2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O��
�ʴ�Ϊ��2Fe2++Cl2=2Fe2++2Cl���� 2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O��
��2�������A��Ԫ���ǵؿ��к�������Ԫ�أ���AΪO��C�ڸ�¯�����еIJμ���Ҫ��Ӧ����CΪCO������BΪCO2��DΪC��C�ڸ�¯�����е���Ҫ��Ӧ�Ļ�ѧ����ʽΪFe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
�ʴ�Ϊ��Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
��3����A�ǵ���ɫ���壬D��������Ԫ����ɵ���ɫ��ζ���壬��AΪNa2O2��DΪCO2��BΪNa2CO3��CΪNaHCO3��Aת��ΪB�Ļ�ѧ����ʽΪ2Na2O2+2 CO2�T2Na2CO3+O2����
�ʴ�Ϊ��2Na2O2+2 CO2�T2Na2CO3+O2����
��4����B��CΪ�����Bת��ΪCʱ����������25%����AӦΪS��BΪSO2��CΪSO3��DΪO2��Bת��ΪC�Ļ�ѧ����ʽ��2SO2+O2$\frac{\underline{����}}{��}$2SO3��
�ʴ�Ϊ��2SO2+O2$\frac{\underline{����}}{��}$2SO3��
��5����DΪǿ�������Һ��A��C����Һ�з�Ӧ���ɰ�ɫ����B����AΪƫ�����Σ�BΪ����������CΪ���Σ�DΪǿ�ᣬ��AΪ���Σ�BΪ����������CΪƫ�����Σ�DΪǿ���ѡ�٢ۣ�
���� ���⿼�����ữ�����ƶϣ��Ƚ�Ϊ�ۺϣ��漰Cl��C��S��NaԪ�ص��ʻ���������ʼ��ת������Ҫѧ���������ջ���֪ʶ���е��Ѷȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 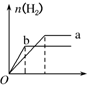 | B�� |  | C�� | 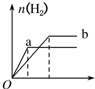 | D�� | 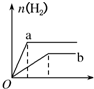 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
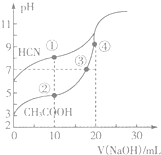 �����£���0.10mol•L-1 NaOH��Һ�ֱ�ζ�20.00mLŨ�Ⱦ�Ϊ0.10mol•L-1��CH3COOH��Һ��HCN��Һ���ζ�������ͼ��ʾ������˵������ȷ���ǣ�������
�����£���0.10mol•L-1 NaOH��Һ�ֱ�ζ�20.00mLŨ�Ⱦ�Ϊ0.10mol•L-1��CH3COOH��Һ��HCN��Һ���ζ�������ͼ��ʾ������˵������ȷ���ǣ�������| A�� | �����Һ��c��CN-���������Һ��c��CH3COO-�� | |
| B�� | �����Һ�У�c��Na+��+c��H+��=c��CH3COO-��+c��OH-�� | |
| C�� | �����Һ�У�c��Na+��=c��CH3COO-��+c��CH3COOH�� | |
| D�� | �����Һ�У�c��Na+����c��CH3COO-����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�32gO2��O3�Ļ����������ԭ����Ϊ2NA | |
| B�� | 0.5mol/L MgCl2��Һ�У�����Cl-������ΪNA | |
| C�� | 2.24L CO��CO2��������к��е�̼ԭ����ĿΪ0.1NA | |
| D�� | 1mol̼�����ӣ�CH 3+�������ĵ�������Ϊ9NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
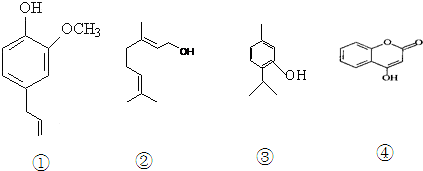
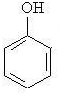 ��
�� 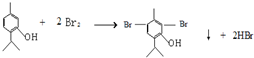 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
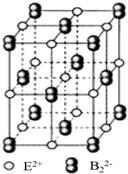 ԭ������С��36��A��B��C��D��E����Ԫ�أ�ԭ��������������A��D���γ�����Һ̬��������ң�ԭ�Ӹ����ȷֱ�Ϊ2��1��1��1��B���γɻ�������������Ԫ�أ�Cԭ�ӻ�̬ʱ2pԭ�ӹ������3��δ�ɶԵĵ��ӣ�E��̬ԭ�ӵĵ�һ�ܲ�������ܲ����ĵ�������ͬ���ڶ��ܲ�������ܲ����ĵ�������ͬ��
ԭ������С��36��A��B��C��D��E����Ԫ�أ�ԭ��������������A��D���γ�����Һ̬��������ң�ԭ�Ӹ����ȷֱ�Ϊ2��1��1��1��B���γɻ�������������Ԫ�أ�Cԭ�ӻ�̬ʱ2pԭ�ӹ������3��δ�ɶԵĵ��ӣ�E��̬ԭ�ӵĵ�һ�ܲ�������ܲ����ĵ�������ͬ���ڶ��ܲ�������ܲ����ĵ�������ͬ��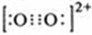 ��1mol D22+�к��еĦм���ĿΪ2NA��
��1mol D22+�к��еĦм���ĿΪ2NA���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
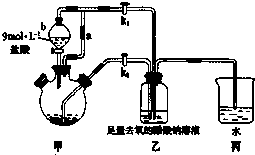 �����Ǹ�ˮ����[Cr��CH3COO��2]2•2H2O����Է�������Ϊ376����һ��Ϊ����ɫ���壬���ױ����������������Ҵ���������ˮ�����ѣ��ӷ����л��ܼ�����
�����Ǹ�ˮ����[Cr��CH3COO��2]2•2H2O����Է�������Ϊ376����һ��Ϊ����ɫ���壬���ױ����������������Ҵ���������ˮ�����ѣ��ӷ����л��ܼ������鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com