
分析 25℃时、有pH为x的HCl溶液和pH为y的NaOH溶液,取VxL该盐酸用该NaOH溶液中和,需VyLNaOH溶液,则有VxL×10-amol/L=VyL×10b-14mol/L,即$\frac{{V}_{x}}{{V}_{y}}$=10x+y-14,以此来计算.
解答 解:25℃时、有pH为x的HCl溶液和pH为y的NaOH溶液,取VxL该盐酸用该NaOH溶液中和,需VyLNaOH溶液,则有VxL×10-xmol/L=VyL×10y-14mol/L,即$\frac{{V}_{x}}{{V}_{y}}$=10x+y-14,
①若x+y=14,则$\frac{{V}_{x}}{{V}_{y}}$=10x+y-14=1:1,故答案为:1:1;
②若x+y=13,则$\frac{{V}_{x}}{{V}_{y}}$=10x+y-14=1:10,故答案为:1:10;
③若x+y>14,则$\frac{{V}_{x}}{{V}_{y}}$=10xy-14>1,即Vx>Vy,故答案为:10x+y-14;>.
点评 本题考查盐类水解和酸碱中和的计算,明确溶液不显电性及原子守恒的关系、酸碱中和时氢离子与氢氧根离子的物质的相同是解答本题的关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
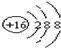 ,Br -的电子式:
,Br -的电子式: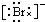 ,CO2的结构式:O=C=O
,CO2的结构式:O=C=O
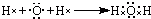 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当a=b>0时,该反应达到化学平衡状态 | |
| B. | 该反应达到化学平衡状态时,一定有a>b | |
| C. | 当密闭容器内气体密度不再改变时,该反应达到化学平衡状态 | |
| D. | 密闭容器中X和Y的物质的量之比为1:2时,该反应达到化学平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳棒上有气体放出,溶液pH变大 | B. | a是正极,b是负极 | ||
| C. | 电子从a极流向b极 | D. | a极上发生了氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去Na2CO3 固体中混有的少量的NaHCO3:置于坩埚中加热 | |
| B. | 除去FeCl2溶液中的FeCl3:加入铁粉 | |
| C. | 除去氢氧化铁胶体中所含的盐酸:过滤 | |
| D. | 除去CO2中混有的少量的HCl:通过饱和的NaHCO3溶液中洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氡是双原子分子 | |
| B. | 氡气因其化学性质活泼而对人体有害 | |
| C. | 氡气因其具有放射性而对人体有害 | |
| D. | 222Rn、219Rn、220Rn是三种同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
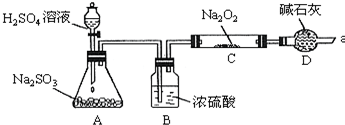

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com