
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 便于消防人员快速通行 | B. | 将可燃物与火源隔离 | ||
| C. | 减少可燃物与空气的接触面积 | D. | 降低可燃物的着火点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5molAl与足量盐酸反应转移电子数为NA | |
| B. | 标准状况下,11.2LSO3所含的分子数为0.5NA | |
| C. | 0.1 mol CH4所含的电子数为NA | |
| D. | 46gNO2和N2O4的混合物含有的分子数为1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
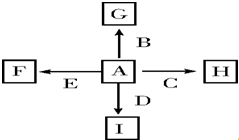 图中A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.
图中A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 可简写为
可简写为  .降冰片烯的分子结构可表示为
.降冰片烯的分子结构可表示为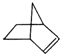
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如图所示,下列关于莽草酸的说法正确的是( )
八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如图所示,下列关于莽草酸的说法正确的是( )| A. | 莽草酸的分子之间可能发生酯化反应 | |
| B. | 莽草酸的分子式为C7H4O5 | |
| C. | 莽草酸中含有苯环 | |
| D. | 莽草酸不能使溴水褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com