
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Ca(OH)2(aq),
Ca(OH)2(aq),A.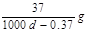 | B.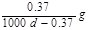 | C.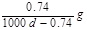 | D.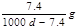 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.混合溶液中c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-) |
| B.混合溶液中c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-) |
| C.加入AgNO3溶液时首先生成AgCl沉淀 |
D.混合溶液中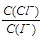 约为1.02×10-3 约为1.02×10-3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1×10-3% | B.2×10-4% | C.9×10-3% | D.2.5×10-20% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
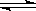 Ag+(aq)+Cl-(aq)溶解平衡,现将足量氯化银分别放入同温下的:①100mL蒸馏水中,②100mL0.1mol·L-1盐酸中,③100mL0.1mol·L-1氯化铝溶液中,④100mL0.1mol·L-1氯化镁溶液中。充分搅拌后,银离子浓度由大到小的顺序是
Ag+(aq)+Cl-(aq)溶解平衡,现将足量氯化银分别放入同温下的:①100mL蒸馏水中,②100mL0.1mol·L-1盐酸中,③100mL0.1mol·L-1氯化铝溶液中,④100mL0.1mol·L-1氯化镁溶液中。充分搅拌后,银离子浓度由大到小的顺序是| A.①②③④ | B.③④①② | C.①②④③ | D.③④②① |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
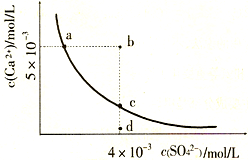
| A.常温下,向100mL CaSO4饱和溶液中,加入400mL 0.01mol/LNa2SO4溶液后,溶液中有沉淀析出 |
| B.b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×10-3 mol/L |
| C.d点溶液通过蒸发可以变到c点 |
| D.a点对应的Ksp等于c点对应的Ksp |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
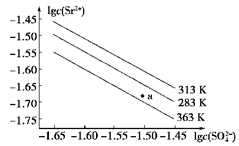
| A.温度一定时,Ksp(SrSO4)随c(SO42—)的增大而减小 |
| B.三个不同温度中,313 K时Ksp(SrSO4)最大 |
| C.283 K时,图中a点对应的溶液是饱和溶液 |
| D.283 K下的SrSO4饱和溶液升温到363 K后变为不饱和溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com