
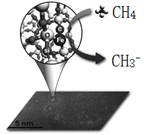
【题目】中科院一项最新成果实现了甲烷高效生产乙烯,甲烷在催化作用下脱氢,在气相中经自由基偶联反应生成乙烯,如图所示。
物质 | 燃烧热(kJ/mol) |
氢气 | 285.8 |
甲烷 | 890.3 |
乙烯 | 1411.5 |
(1)已知相关物质的燃烧热如上表,写出甲烷制备乙烯的热化学方程式_________。
(2)在400℃时,向1L的恒容反应器中充入1molCH4,发生上述反应,测得平衡混合气体中C2H4的体积分数为20.0 %。则在该温度下,其平衡常数K=_______。按化学平衡移动原理,在图(a)中画出该反应的平衡转化率与温度及压强(p1>p2)的关系曲线。_______________________
(3)在制备C2H4时,通常存在副反应:2CH4(g)![]() C2H6(g)+H2(g)。在常温下,向体积为1L的恒容反应器中充入1molCH4,然后不断升高温度,得到图(b)。
C2H6(g)+H2(g)。在常温下,向体积为1L的恒容反应器中充入1molCH4,然后不断升高温度,得到图(b)。
①在200℃时,测出乙烷的量比乙烯多的主要原因是_________________________。
②在600℃后,乙烯的体积分数减少的主要原因是__________________________。

(4)工业上常采用除杂效率高的吸收-电解联合法,除去天然气中的杂质气体H2S,并转化为可回收利用的单质硫,其装置如下图所示。

通电前,先通入一段时间含H2S的甲烷气,使部分NaOH吸收H2S转化为Na2S,再接通电源,继续通入含杂质的甲烷气,并控制好通气速率。装置中右端碳棒为_________极,左端碳棒上的电极反应为_________________________,右池中的c(NaOH):c(Na2S)______________(填“增大”、“基本不变”或“减小)。
【答案】 2CH4(g)![]() C2H4(g)+2H2(g) ΔH=+202.5 kJ/mol 0.25
C2H4(g)+2H2(g) ΔH=+202.5 kJ/mol 0.25 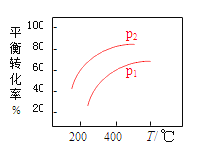 在200℃时,乙烷的生成速率比乙烯的快 在600℃后,乙烯开始分解为碳和氢气 阳 2H2O+2e-=2OH-+H2↑或2H++2e-=H2↑ 基本不变
在200℃时,乙烷的生成速率比乙烯的快 在600℃后,乙烯开始分解为碳和氢气 阳 2H2O+2e-=2OH-+H2↑或2H++2e-=H2↑ 基本不变
【解析】(1)根据燃烧热数据表可得:①H2(g)+ ![]() O2(g)=H2O(l) ΔH1=-285.8kJ/mol;②CH4(g) + 2O2(g)=CO2(g)+2H2O(l) ΔH2=-890. 3kJ/mol; ③C2H4(g) + 3O2(g)=2CO2(g)+2H2O(l) ΔH3=-1411.0kJ/mol;根据盖斯定律,由②×2-③-①×2得反应2CH4(g)
O2(g)=H2O(l) ΔH1=-285.8kJ/mol;②CH4(g) + 2O2(g)=CO2(g)+2H2O(l) ΔH2=-890. 3kJ/mol; ③C2H4(g) + 3O2(g)=2CO2(g)+2H2O(l) ΔH3=-1411.0kJ/mol;根据盖斯定律,由②×2-③-①×2得反应2CH4(g)![]() C2H4(g)+2H2(g) ΔH=ΔH2×2-ΔH3-ΔH1×2=-890. 3kJ/mol×2-(-1411.0kJ/mol)-(-285.8kJ/mol)×2=+202.2 kJ/mol;(2)在400℃时,向1L的恒容反应器中充入1molCH4,发生反应2CH4(g)
C2H4(g)+2H2(g) ΔH=ΔH2×2-ΔH3-ΔH1×2=-890. 3kJ/mol×2-(-1411.0kJ/mol)-(-285.8kJ/mol)×2=+202.2 kJ/mol;(2)在400℃时,向1L的恒容反应器中充入1molCH4,发生反应2CH4(g)![]() C2H4(g)+2H2(g),测得平衡混和气体中C2H4的体积分数为20.0%。设甲烷的转化率为x,则:
C2H4(g)+2H2(g),测得平衡混和气体中C2H4的体积分数为20.0%。设甲烷的转化率为x,则:
2CH4(g)![]() C2H4(g)+2H2(g)
C2H4(g)+2H2(g)
起始浓度(mol/L) 1 0 0
改变浓度(mol/L) x x/2 x
平衡浓度(mol/L) 1-x x/2 x
相同条件下,气体的物质的量之比等于体积之比,则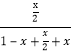 =20.0%,解得x=0.5mol/L,K=
=20.0%,解得x=0.5mol/L,K=![]() =0.25;按化学平衡移动原理,该反应正反应为气体体积增大的吸热反应,升高温度平衡正向移动,平衡转化率增大,增大压强,平衡逆向移动,平衡转化率减小,对应图中曲线为(p1>p2):
=0.25;按化学平衡移动原理,该反应正反应为气体体积增大的吸热反应,升高温度平衡正向移动,平衡转化率增大,增大压强,平衡逆向移动,平衡转化率减小,对应图中曲线为(p1>p2):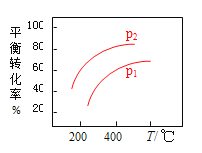 ;(3)①根据图中曲线可知,在200℃时,乙烷的生成速率比乙烯的快,测出乙烷的量比乙烯多;②在600℃后,乙烯开始分解为碳和氢气,乙烯的体积分数减少;(4)装置中右端硫离子失电子转化为硫单质,硫元素被还原,则右端碳棒为阳极,左端碳棒为阴极产生氢气,阴极的电极反应为:2H2O+2e-=2OH-+H2↑;因接通电源,继续通入含杂质的甲烷气,并控制好通气速率。故右池中的c(NaOH):c(Na2S)基本不变。
;(3)①根据图中曲线可知,在200℃时,乙烷的生成速率比乙烯的快,测出乙烷的量比乙烯多;②在600℃后,乙烯开始分解为碳和氢气,乙烯的体积分数减少;(4)装置中右端硫离子失电子转化为硫单质,硫元素被还原,则右端碳棒为阳极,左端碳棒为阴极产生氢气,阴极的电极反应为:2H2O+2e-=2OH-+H2↑;因接通电源,继续通入含杂质的甲烷气,并控制好通气速率。故右池中的c(NaOH):c(Na2S)基本不变。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 硬脂酸甘油酯在NaOH溶液中水解完全后,加入饱和食盐水,下层析出硬脂酸钠
B. 乙酸的分子模型可表示为![]()
C. 石油分馏是物理变化,可得到汽油、煤油和柴油等产品
D. 相同物质的量的C3H6和C3H8O,充分燃烧,消耗氧气量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ga、As、Al、C的相关化合物在化工和医学领域有着广泛的应用。回答下列问题:
(1)写出基态Ga原子的核外电子排布式:_________,有_____个未成对电子。
(2)合金砷化镓在现代工业中被广泛应用,Ga、As电负性由大到小排序为______________。
(3)1个丙二烯分子中σ键总数为___个,C原子的杂化方式为______。分子中的大π键可以用符号пmn表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为п66),则丙二烯中的大π键应表示为____________。
(4)氮化镓是第三代半导体材料,其晶体结构和单晶硅相似,晶胞结构如图所示:

①原子坐标参数是表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0, 0, 0);B为(1/2,1/2,0);C为(1,0,1)。则D原子的坐标参数为_________________。
②已知氮化镓晶胞的边长为a nm,其密度为d g/cm3,则阿伏加德罗常数NA =____(用a、d表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比推理是重要的学科思想,下列根据已知进行推理正确的是( )
选项 | 已知 | 类比推理 |
A |
|
|
B |
|
|
C | 常温下,浓硝酸使铁钝化 | 浓硝酸与铜不反应 |
D |
| 过量 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若将反应:Zn+H2SO4=ZnSO4+H2↑设计成原电池(装置如图),则下列说法正确的是( ) 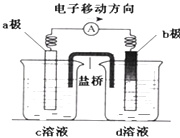
A.d溶液是稀硫酸
B.c溶液颜色变蓝
C.b极发生氧化反应
D.a极是铜棒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、R、M的原子序数依次增大,其中只有R属于金属元素,由X、Y、R可组成一种化合物Q,在298K时,0.1mol·L—1 Q溶液的AG(酸度)=lg![]() =-12,由X和M组成的化合物XM是强电解质。下列说法正确的是
=-12,由X和M组成的化合物XM是强电解质。下列说法正确的是
A. Y、R、M三种元素形成的简单离子半径:r(M)>r(R)>r(Y)
B. M的氧化物对应的水化物一定是强酸
C. R分别与X、Y、M组成的二元化合物中都含有离子键
D. 化合物RYX和RMY均能抑制水的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体V L(标准状况),向反应后的溶液中(存在Cu2+和SO42﹣)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO 12.0g,若上述气体为NO和NO2的混合物,且体积比为1:1,则V可能为( )
A.7.5 L
B.12.3 L
C.15.7 L
D.16.8 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,发生如下反应:2SO2(g)+O2(g) ![]() 2SO3(g)ΔH<0。改变起始时n(SO2)对反应的影响如图所示。下列说法正确的是
2SO3(g)ΔH<0。改变起始时n(SO2)对反应的影响如图所示。下列说法正确的是
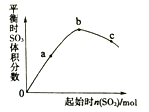
A. SO2的起始量越大,混合气体中SO2的体积分数越大
B. a、b、c三点中,a点时SO2的转化率最高
C. a、b、c三点的平衡常数:Kb>Kc>Ka
D. b、c点均为化学平衡点,a点未达平衡且反应正向进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com