
| A. | 用少量水稀释0.1mol•L-1氨水时,溶液中$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$减小 | |
| B. | 将Na2CO3溶液从20℃升温至30℃,溶液中增大$\frac{c(C{{O}_{3}}^{2-})}{c(HC{{O}_{3}}^{-})•c(O{H}^{-})}$增大 | |
| C. | 向NH4Cl溶液中加入NaOH溶液至呈中性,溶液中c(Na+)=c(NH3•H2O) | |
| D. | pH=5.5的CH3COOH与CH3COONa混合溶液中c(Na+)>c(CH3COO-) |
分析 A.用水稀释0.1mol/L氨水时,加水稀释,促进氨水电离,n(OH-)增大,n(NH3.H2O)减少;
B.根据将Na2CO3溶液从20℃升温至30℃,水解程度增大即反应物离子变少,生成物离子增多判断;
C.根据电荷守恒结合NH4Cl溶液中的物料守恒判断;
D.根据pH=5.5的CH3COOH与CH3COONa混合溶液中电荷守恒判断.
解答 解:A.加水稀释,促进氨水电离,n(OH-)增大,n(NH3.H2O)减少,所以$\frac{\frac{n(OH{\;}^{-})}{V}}{\frac{n(NH{\;}_{3}.H{\;}_{2}O)}{V}}$增大,即$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$增大,故A错误;
B.Na2CO3溶液从20℃升温至30℃,水解程度增大,所以碳酸根离子的物质的量减小,水解生成的碳酸氢根和氢氧根物质的量都增大,又在同一溶液中,体积相等,所以$\frac{c(C{{O}_{3}}^{2-})}{c(HC{{O}_{3}}^{-})•c(O{H}^{-})}$减小,故B错误;
C.向NH4Cl溶液中加入NaOH溶液至呈中性,根据电荷守恒,则有c(NH4+)+c(Na+)=c(Cl-),又NH4Cl溶液中物料守恒,(Cl-)=c(NH4+)+c(NH3•H2O),所以c(Na+)=c(NH3•H2O),故C正确;
D.pH=5.5的CH3COOH与CH3COONa混合溶液中,根据电荷守恒,则有c(Na+)+c(H+)=c(CH3COO-)+c(OH-),又pH=5.5,c(H+)>c(OH-),所以c(Na+)<c(CH3COO-),故D错误;
故选C.
点评 本题对弱电解质的电离及其盐类的水解与离子浓度大小比较、酸碱混合溶液定性判断联合考查,结合物料守恒和电荷守恒解答即可,难度中等.


科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
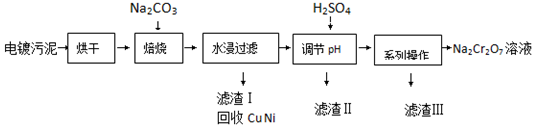
| 20℃ | 60℃ | 100℃ | |
| Na2SO4 | 19.5 | 45.3 | 42.5 |
| Na2Cr2O7 | 183 | 269 | 415 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4、9、24、14、28 | B. | 1、1、1、1、2 | C. | 8、9、12、10、20 | D. | 任意比均可 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
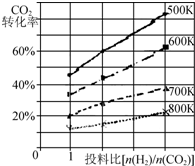 将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(g);△H
将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(g);△H查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当电池正极消耗mg气体时,电解池阴极同时有mg气体生成 | |
| B. | 电解后c(Na+)与c(CO32-)的比值变小 | |
| C. | 电池中c(KOH)不变;电解池中溶液pH变大 | |
| D. | 电解后c(Na2CO3)不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com