
| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| NO�����ʵ�����mol�� | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
| ���� | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| ������kJ�� | 243 | 193 | 151 | 431 | 366 | 298 | 436 |
���� ��1�����ݱ�������֪��3sʱ�÷�Ӧ�Ѿ��ﵽƽ��״̬����3s��5sʱNOת������ȣ�3sʱ�μӷ�Ӧ��n��NO��=��0.020-0.007��mol=0.013mol��NOת����=$\frac{�μӷ�Ӧ��n��NO��}{��ʼn��NO��}$��100%��
��2��v��NO��=$\frac{\frac{0.020-0.010}{2l}}{2s}$=0.0025mol/��L•s����ͬһ���淴Ӧ��ͬһ��ʱ���ڸ����ʵķ�Ӧ����֮�ȵ����������֮�ȼ�������ƽ����Ӧ���ʣ�
��3�����淴Ӧ�ﵽƽ��״̬ʱ��ͬһ���ʵ����淴Ӧ������ȣ���Ӧ��ϵ�и����ʵ����ʵ��������ʵ���Ũ�ȡ��ٷֺ������ɴ������һϵ�����������䣻
��4���ƻ�1mol �����еĻ�ѧ�������ĵ�����Խ����˵������Խ�ȶ������ʾ��е�����Խ�ͣ�
��5�������ƻ�1 mol�����еĻ�ѧ�������ĵ�����Խ��������Խ�ȶ���
��6���γ��¼��ͷŵ������;ɼ��������յ����������ж�
��� �⣺��1�����ݱ�������֪��3sʱ�÷�Ӧ�Ѿ��ﵽƽ��״̬����3s��5sʱNOת������ȣ�3sʱ�μӷ�Ӧ��n��NO��=��0.020-0.007��mol=0.013mol��NOת����=$\frac{�μӷ�Ӧ��n��NO��}{��ʼn��NO��}$��100%=$\frac{0.013mol}{0.020mol}$��100%=65%��
�ʴ�Ϊ��65%��
��2��v��NO��=$\frac{\frac{0.020-0.010}{2l}}{2s}$=0.0025mol/��L•s����ͬһ���淴Ӧ��ͬһ��ʱ���ڸ����ʵķ�Ӧ����֮�ȵ����������֮�ȣ�����v��O2��=$\frac{1}{2}$v��NO��=$\frac{1}{2}$��0.0025mol/��L•s��=0.0012 5 mol/��L•s����
�ʴ�Ϊ��0.0012 5 mol/��L•s����
��3��a��v��NO2��=2v��O2��û����ȷ��Ӧ�������Բ��ܾݴ��ж�ƽ��״̬���ʴ���
b����Ӧǰ����������ʵ�����С����������ѹǿ��С����������ѹǿ���ֲ���ʱ�������ʵ����ʵ������䣬��Ӧ�ﵽƽ��״̬������ȷ��
c��v����NO��=2v����O2��=v����NO����NO���淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬������ȷ��
d����Ӧǰ���������������䣬����������䣬�����ܶ�ʼ�ղ��䣬���ܾݴ��ж�ƽ��״̬���ʴ���
��ѡbc��
��4�����ݱ������ݿ�֪���ƻ�1molCl2�еĻ�ѧ�������ĵ�����Ϊ234KJ���ƻ�1molBr2�еĻ�ѧ�������ĵ�����Ϊ193KJ���ƻ�1molI2�еĻ�ѧ�������ĵ�����Ϊ151KJ���ƻ�1molH2�еĻ�ѧ�������ĵ�����Ϊ436KJ�������ƻ�1molH2����������ͣ����ȶ���H2�������е�������ͣ�
��ѡ��A��
��5�����ݱ������ݿ�֪���ƻ�1molHCl�еĻ�ѧ�������ĵ�������ߣ���˵��HCl���ȶ���
�ʴ�Ϊ��HCl��
��6�����ݷ�ӦX2+H2�T2HX�����Լ����¼������ͷŵ����������ھɼ��������յ�����������X2+H2�T2HX�ķ�Ӧ�Ƿ��ȷ�Ӧ��
�ʴ�Ϊ�����ȷ�Ӧ��
���� ���⿼�黯ѧƽ����㼰��Ӧ�ȵ��йؼ��㣬Ϊ��Ƶ���㣬���ؿ���ѧ����������������ע�⣺ֻ�з�Ӧǰ��ı��������������Ϊ���淴Ӧƽ��״̬�ж����ݣ�ע��II�����������������ȶ��ԵĹ�ϵ����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 13��8 | B�� | 8��13 | C�� | 16��9 | D�� | 9��16 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
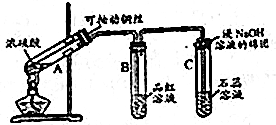
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
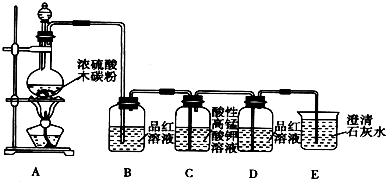
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
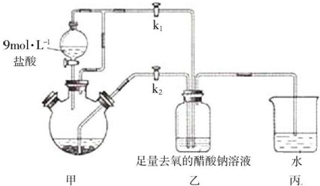
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
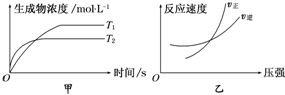
| A�� | a+b��c+d��T1��T2��H��0 | B�� | a+b��c+d��T1��T2 ��H��0 | ||
| C�� | a+b��c+d��T1��T2��H��0 | D�� | a+b��c+d��T1��T2��H��0 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com