

 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
| A、1mol聚乙烯含有的原子数目为6NA |
| B、标准状况下,11.2L二氯甲烷所含分子数为0.5NA |
| C、2.8g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| D、1mol甲基含10NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
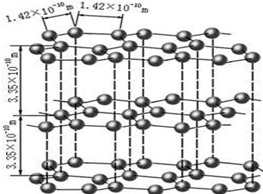
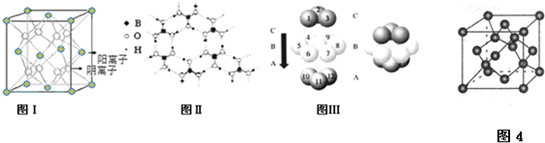
查看答案和解析>>
科目:高中化学 来源: 题型:
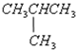 ;⑥石墨;⑦14C;⑧CO2.
;⑥石墨;⑦14C;⑧CO2.查看答案和解析>>
科目:高中化学 来源: 题型:

| 编号 | a | b | c | d |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 解释或实验结论 |
| (1)测得A蒸汽的摩尔质量是同状况下甲烷的4.375倍 | 试通过计算填空: (1)A的相对分子质量为 |
| (2)将5.6g A在足量O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重7.2g和17.6g | (2)A的分子式为 |
| (3)将A通入溴水中,溴水褪色 | (3)说明A属于 烯 烃类 |
| (4)经红外光谱法测定A分子结构中只含两个甲基 | (4)写出其可能的结构简式 |
查看答案和解析>>
科目:高中化学 来源: 题型:
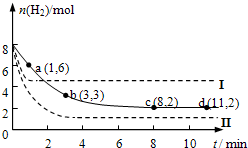 固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+Q(Q>0)某科学实验小组将6mol CO2和8mol H2充入一容积为2L的密闭容器中(温度保持不变),测得H2的物质的量随时间变化如下图中实线所示(图中字母后的数字表示对应的坐标).回答下列问题:
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+Q(Q>0)某科学实验小组将6mol CO2和8mol H2充入一容积为2L的密闭容器中(温度保持不变),测得H2的物质的量随时间变化如下图中实线所示(图中字母后的数字表示对应的坐标).回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| A、难氧化、难取代、难加成 |
| B、易氧化、易取代、易加成 |
| C、难氧化、易取代、难加成 |
| D、易氧化、易取代、难加成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com