


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案科目:高中化学 来源: 题型:阅读理解
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
aFe+bNO![]() +cH+
+cH+![]() dFe2++fFe3++g NO↑+hN2O↑+kH2O(化学计量数均为正整数)。回答下列问题:(1)根据反应中氮、氢、氧三种元素的原子个数守恒,可得c、g、h的关系式是 (用一个代数式表示。下同)。?
dFe2++fFe3++g NO↑+hN2O↑+kH2O(化学计量数均为正整数)。回答下列问题:(1)根据反应中氮、氢、氧三种元素的原子个数守恒,可得c、g、h的关系式是 (用一个代数式表示。下同)。?
(2)根据反应中离子电荷守恒,可得b、c、d、f的关系式是 。
(3)根据反应中电子转移的总数相等,可得d、f、g、h的关系式是 ,若a等于12,且铁和稀硝酸恰好完全反应,则b的取值范围是 ,c的取值范围是 。?
查看答案和解析>>
科目:高中化学 来源: 题型:
已知单质铁溶于一定浓度的硝酸溶液中,反应的离子方程式为:?
aFe+bNO![]() +cH+
+cH+![]() dFe2++fFe3++g NO↑+hN2O↑+kH2O(化学计量数均为正整数)。回答下列问题:(1)根据反应中氮、氢、氧三种元素的原子个数守恒,可得c、g、h的关系式是 (用一个代数式表示。下同)。?
dFe2++fFe3++g NO↑+hN2O↑+kH2O(化学计量数均为正整数)。回答下列问题:(1)根据反应中氮、氢、氧三种元素的原子个数守恒,可得c、g、h的关系式是 (用一个代数式表示。下同)。?
(2)根据反应中离子电荷守恒,可得b、c、d、f的关系式是 。
(3)根据反应中电子转移的总数相等,可得d、f、g、h的关系式是 ,若a等于12,且铁和稀硝酸恰好完全反应,则b的取值范围是 ,c的取值范围是 。?
查看答案和解析>>
科目:高中化学 来源:江苏模拟题 题型:填空题
 (NH4)2S2O8 + H2↑;(NH4)2S2O8 + 2H2O = 2NH4HSO4 + H2O2
(NH4)2S2O8 + H2↑;(NH4)2S2O8 + 2H2O = 2NH4HSO4 + H2O2 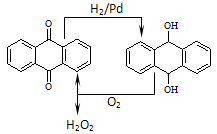
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com