
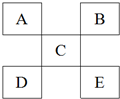
| A. | 如果D是金属元素,那么D元素的金属性比C强 | |
| B. | 元素C的最高价氧化物对应的水化物一定是强酸 | |
| C. | 元素B与氢形成的化合物中只能存在极性共价键 | |
| D. | 若E为非金属,则E的非金属性要强于B |
分析 图是元素周期表的一部分,其中A、B、C为短周期主族元素,可知A、B处于第二周期,C处于第三周期,D、E处于第四周期.
A.同周期自左而右金属性减弱,同主族自上而下金属性增强;
B.C元素可以为Si、P、S等元素;
C.元素B可以为O元素,与氢形成可以形成水、过氧化氢;
D.同主族自上而下非金属性减弱.
解答 解:图是元素周期表的一部分,其中A、B、C为短周期主族元素,可知A、B处于第二周期,C处于第三周期,D、E处于第四周期.
A.同周期自左而右金属性减弱,同主族自上而下金属性增强,如果D是金属元素,那么D元素的金属性比C强,故A正确;
B.C元素可以为Si、P、S等元素,硅酸、硫酸不属于强酸,故B错误;
C.元素B可以为O元素,与氢形成可以形成水、过氧化氢,过氧化氢中含有非极性键,故C错误;
D.同主族自上而下非金属性减弱,若E为非金属,则E的非金属性要弱于B,故D错误.
故选:A.
点评 本题考查元素周期表与元素周期律综合运用,侧重对元素周期律的考查,熟练掌握元素周期表的结构与元素化合物性质.


科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用溴水检验CH2═CH-CHO中是否含有碳碳双键 | |
| B. | 1 mol HCHO发生银镜反应最多生成2 mol Ag | |
| C. | 对甲基苯甲醛( )使酸性高锰酸钾溶液褪色,说明它含有醛基 )使酸性高锰酸钾溶液褪色,说明它含有醛基 | |
| D. | 能发生银镜反应的有机物不一定是醛类 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
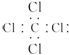
| A. | 全对 | B. | 全错 | C. | ③④ | D. | ①⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 原子序数小于36的X、Y、Z、W、R五种元素,原子序数依次增大.五种元素中,仅R为金属元素,其原子序数为27.X价电子排布式为nsnnpn,元素Z基态原子s电子总数与p电子总数相等,W与其它四种元素能层数不同,且未成对电子数目为1个.
原子序数小于36的X、Y、Z、W、R五种元素,原子序数依次增大.五种元素中,仅R为金属元素,其原子序数为27.X价电子排布式为nsnnpn,元素Z基态原子s电子总数与p电子总数相等,W与其它四种元素能层数不同,且未成对电子数目为1个.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
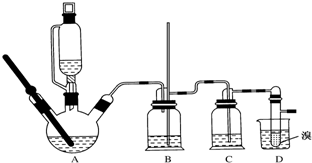
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状 态 | 无 色 液 体 | 无 色 液 体 | 无 色 液 体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何反应中的能量变化都表现为热量变化 | |
| B. | 任何化学反应都伴随着能量变化 | |
| C. | 反应物的总能量高于生成物的总能量,则反应释放能量 | |
| D. | 若化学键形成时释放的能量小于破坏旧化学键时所需要吸收的能量,则反应吸收能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
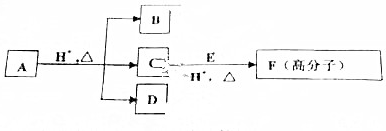
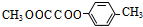 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com