
【题目】冠醚分子中有空穴 ,能够与金属离子形成稳定的络合物,该物质在有机工业中发挥着重要的作用。二环己烷并一18一冠一6(III )的制备原理如图,下列相关说法错误的是
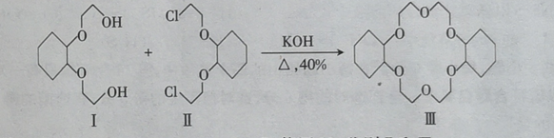
A.反应是取代反应B.能用Na鉴别I和III
C.I不能使酸性高锰酸钾溶液褪色D.III的一溴取代物有5种
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案科目:高中化学 来源: 题型:
【题目】某温度下,相同pH的两种弱酸HA和HB分别加水稀释,pH随溶液体积变化的曲线如图所示。下列判断正确的是( )
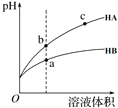
A.酸性:HB> HA
B.结合H+的能力:B->A-
C.导电能力:c > b
D.与氢氧化钠完全反应时,消耗氢氧化钠体积Va<Vb
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把在空气中久置的铝片5.0 g投入盛有 500 mL 0.5 mol·L-1的硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图的坐标曲线来表示,回答下列问题:
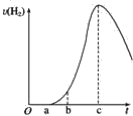
(1)曲线由O→a段不产生氢气的原因是__________________;
(2)曲线由a→c段,产生氢气的速率增加较快的主要原因是______________;
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因是_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100 ℃时,将0.100 mol的N2O4气体充入1 L 抽空的密闭容器中,发生如下反应:N2O4![]() 2NO2,隔一定时间对该容器内的物质进行分析,得到下表:
2NO2,隔一定时间对该容器内的物质进行分析,得到下表:
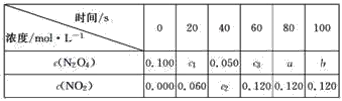
(1)达到平衡时,N2O4的转化率为______________,表中c2________c3,a________b(填“>”、“<”或“=”)。
(2)20 s时N2O4的浓度c1=________ mol·L-1,在0~20 s内N2O4的平均反应速率为________ mol·L-1·s-1。
(3)若在相同情况下最初向该容器充入的是二氧化氮气体,则要达到上述同样的平衡状态,二氧化氮的起始浓度是________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】冠病毒(如图)由蛋白质和核酸组成,核酸由核苷酸组成.核苷酸的单体由五碳糖 、磷酸基和含氮碱基构成.下列说法错误的是
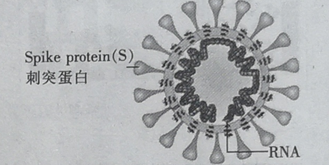
A.蛋白质和核酸均是高分子化合物
B.蛋白质中含C、H、O、N 等元素
C.五碳糖( C5H10O5)与葡萄糖互为同系物
D.NaClO溶液用作消毒剂,是因为NaClO 能使病毒蛋白变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式氯化铜[CuaClb(OH)c·xH2O]制备需要的CuCl2可用Fe3+作催化剂得到,其催化原理如图所示. 下列有关说法正确的是

A.a、b、c 之间的关系式为:a=b+c
B.图中M、N分别为Fe2+、Fe3+
C.若制备1 mol的CuCl2,理论上消耗11.2 LO2
D.N参加的反应离子方程式为:4Fe2++ O2+ 4H+ = 4Fe3+ + 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,H2S 的 Ka1 =1.0 ×10-7,Ka2 =1.0 ×10-15下列说法正确的是
A.0.1 mol L-1的 NaHS溶液中:c(S2ˉ)>c(H2S)
B.反应 S2ˉ+ H2O ![]() HSˉ+ OHˉ 的平衡常数 K=1×10-7
HSˉ+ OHˉ 的平衡常数 K=1×10-7
C.NaHS与 Na2S以任意比混合的溶液中 :c( Na+)+ c(H+)=c(HSˉ)+ c(S2ˉ)+c(OHˉ)
D.0.1 mol L-1的Na2S 溶液中:c(OHˉ)= c(H+)+ c(HSˉ) + 2c(H2S)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
①CO(g)+1/2O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
②H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
下列说法正确的是( )
A. 通常状况下,氢气的燃烧热为241.8 kJ·mol-1
B. 由①可知,1 mol CO(g)和1/2 mol O2(g)反应生成 1 mol CO2(g),放出283.0 kJ的热量
C. 可用右图表示2CO2(g)===2CO(g)+O2(g)反应过程中的能量变化关系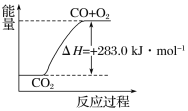
D. 分解1 mol H2O(g),其反应热为-241.8 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容的密闭容器中进行下列可逆反应:C(s)+H2O(g)![]() CO(g)+H2(g);现有下列状态:①混合气体的密度不再改变;②各气体的浓度相等;③反应体系中温度保持不变(假设为绝热容器);④相同时间内,断裂H—O键的速率是断裂H—H键速率的2倍;其中能表明反应达到平衡状态的是
CO(g)+H2(g);现有下列状态:①混合气体的密度不再改变;②各气体的浓度相等;③反应体系中温度保持不变(假设为绝热容器);④相同时间内,断裂H—O键的速率是断裂H—H键速率的2倍;其中能表明反应达到平衡状态的是
A.①②③B.②③C.②③④D.①③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com